Умеренно выраженный перифокальный отек
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ПОРАЖЕНИЙ БЕЛОГО ВЕЩЕСТВА
Дифференциально-диагностический ряд заболеваний белого вещества является очень длинным. Выявленные с помощью МРТ очаги могут отражать нормальные возрастные изменения, но большинство очагов в белом веществе возникают в течение жизни и в результате гипоксии и ишемии.
Рассеянный склероз считается самым распространенным воспалительным заболеванием, которое характеризуется поражением белого вещества головного мозга. Наиболее частыми вирусными заболеваниями, приводящими к возникновению похожих очагов, являются прогрессирующая мультифокальная лейкоэнцефалопатия и герпесвирусная инфекция. Они характеризуются симметричными патологическими участками, которые нужно дифференцировать с интоксикациями.
Сложность дифференциальной диагностики обусловливает в ряде случаев необходимость дополнительной консультации с нейрорадиологом с целью получения второго мнения.
ПРИ КАКИХ БОЛЕЗНЯХ ВОЗНИКАЮТ ОЧАГИ В БЕЛОМ ВЕЩЕСТВЕ?
Очаговые изменения сосудистого генеза
- Атеросклероз
- Гипергомоцистеинемия
- Амилоидная ангиопатия
- Диабетическая микроангиопатия
- Гипертония
- Мигрень
Воспалительные заболевания
- Рассеянный склероз
- Васкулиты: системная красная волчанка, болезнь Бехчета, болезнь Шегрена
- Саркоидоз
- Воспалительные заболевания кишечника (болезнь Крона, язвенный колит, целиакия)
Заболевания инфекционной природы
- ВИЧ, сифилис, боррелиоз (болезнь Лайма)
- Прогрессирующая мультифокальная лейконцефалопатия
- Острый рассеянный (диссеминированный) энцефаломиелит (ОДЭМ)
Интоксикации и метаболические расстройства
- Отравление угарным газом, дефицит витамина B12
- Центральный понтинный миелинолиз
Травматические процессы
- Связанные с лучевой терапией
- Постконтузионные очаги
Врожденные заболевания
- Обусловленные нарушением метаболизма (имеют симметричный характер, требуют дифференциальной диагностики с токсическими энцефалопатиями)
Могут наблюдаться в норме
- Перивентрикулярный лейкоареоз, 1 степень по шкале Fazekas
МРТ ГОЛОВНОГО МОЗГА: МНОЖЕСТВЕННЫЕ ОЧАГОВЫЕ ИЗМЕНЕНИЯ
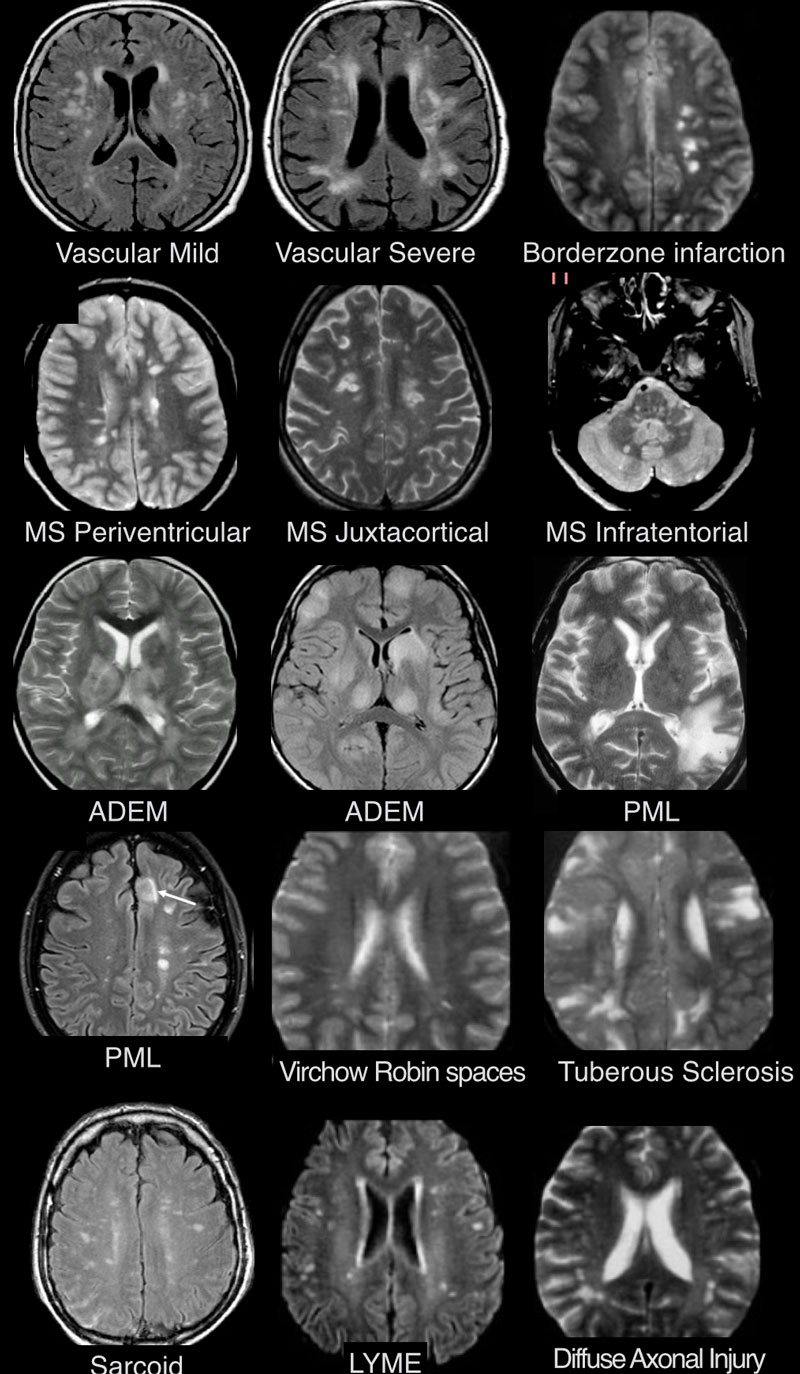
На изображениях определяются множественные точечные и «пятнистые» очаги. Некоторые из них будут рассмотрены более детально.
Инфаркты по типу водораздела
- Главное отличие инфарктов (инсультов) этого типа — это предрасположенность к локализации очагов только в одном полушарии на границе крупных бассейнов кровоснабжения. На МР-томограмме представлен инфаркт в бассейне глубоких ветвей.
Острий диссеминированный энцефаломиелит (ОДЭМ)
- Основное отличие: появление мультифокальных участков в белом веществе и в области базальных ганглиев через 10-14 дней после перенесенной инфекции или вакцинации. Как при рассеянном склерозе, при ОДЭМ может поражаться спинной мозг, дугообразные волокна и мозолистое тело; в некоторых случаях очаги могут накапливать контраст. Отличием от РС считается тот момент, что они имеют большой размер и возникают преимущественно у молодых пациентов. Заболевание отличается монофазным течением
Болезнь Лайма
- Характеризуется наличием мелких очажков размером 2-3 мм, имитирующих таковые при РС, у пациента с кожной сыпью и гриппоподобным синдромом. Другими особенностями являются гиперинтенсивный сигнал от спинного мозга и контрастное усиление в области корневой зоны седьмой пары черепно-мозговых нервов.
Саркоидоз головного мозга
- Распределение очаговых изменений при саркоидозе крайне напоминает таковое при рассеянном склерозе.
Прогрессирующая мультфокальная лейкоэнцефалопатия (ПМЛ)
- Демиелинизирующее заболевание, обусловленное вирусом Джона Каннигема у пациентов с иммунодефицитом. Ключевым признаком являются поражения белого вещества в области дугообразных волокон, не усиливающиеся при контрастировании, оказывающие объемное воздействие (в отличие от поражений, обусловленных ВИЧ или цитомегаловирусом). Патологические участки при ПМЛ могут быть односторонними, но чаще они возникают с обеих сторон и являются асимметричными.
Пространства Вирхова-Робина
- Ключевой признак: гиперинтенсивный сигнал на Т2 ВИ и гипоинтенсивный на FLAIR
Сосудистые очаги
- Для зон сосудистого характера типична глубокая локализация в белом веществе, отсутствие вовлечения мозолистого тела, а также юкставентрикулярных и юкстакортикальных участков.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА МНОЖЕСТВЕННЫХ ОЧАГОВ, УСИЛИВАЮЩИХСЯ ПРИ КОНТРАСТИРОВАНИИ
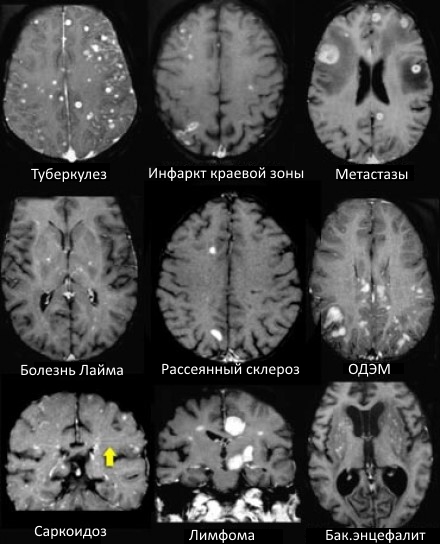
На МР-томограммах продемонстрированы множественные патологические зоны, накапливающие контрастное вещество. Некоторые из них описаны далее подробнее.
Васкулиты
- Большинство васкулитов характеризуются возникновением точечных очаговых изменений, усиливающихся при контрастировании. Поражение сосудов головного мозга наблюдается при системной красной волчанке, паранеопластическом лимбическом энцефалите, б. Бехчета, сифилисе, гранулематозе Вегенера, б. Шегрена, а также при первичных ангиитах ЦНС.
Болезнь Бехчета
- Чаще возникает у пациентов турецкого происхождения. Типичным проявлением этого заболевания признано вовлечение мозгового ствола с появлением патологических участков, усиливающихся при контрастировании в острой фазе.
Метастазы
- Характеризуются выраженным перифокальным отеком.
Инфаркт по типу водораздела
- Периферические инфаркты краевой зоны могут усиливаться при контрастировании на ранней стадии.
ПЕРИВАСКУЛЯРНЫЕ ПРОСТРАНСТВА ВИРХОВА-РОБИНА
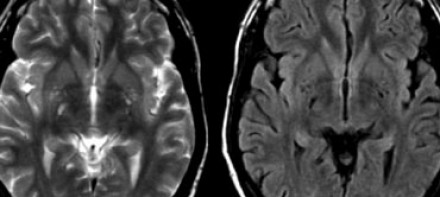
Слева на Т2-взвешенной томограмме видны множественные очаги высокой интенсивности в области базальных ганглиев. Справа в режиме FLAIR сигнал от них подавляется, и они выглядят темными. На всех остальных последовательностях они характеризуются такими же характеристиками сигнала, как ликвор (в частности, гипоинтенсивным сигналом на Т1 ВИ). Такая интенсивность сигнала в сочетании с локализацией описанного процесса являются типичными признаками пространств Вирхова-Робина (они же криблюры).
Пространства Вирхова-Робина окружают пенетрирующие лептоменингеальные сосуды, содержат ликвор. Их типичной локализацией считается область базальных ганглиев, характерно также расположение вблизи передней комиссуры и в центре мозгового ствола. На МРТ сигнал от пространств Вирхова-Робина на всех последовательностях аналогичен сигналу от ликвора. В режиме FLAIR и на томограммах, взвешенных по протонной плотности, они дают гипоинтенсивный сигнал в отличие от очагов иного характера. Пространства Вирхова-Робина имеют небольшие размеры, за исключением передней комиссуры, где периваскулярные пространства могут быть больше.
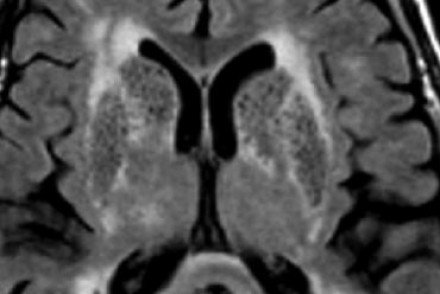
На МР-томограмме можно обнаружить как расширенные периваскулярные пространства Вирхова-Робина, так и диффузные гиперинтенсивные участки в белом веществе. Данная МР-томограмма превосходно иллюстрирует различия между пространствами Вирхова-Робина и поражениями белого вещества. В данном случае изменения выражены в значительной степени; для их описания иногда используется термин «ситовидное состояние» (etat crible). Пространства Вирхова-Робина увеличиваются с возрастом, а также при гипертонической болезни в результате атрофического процесса в окружающей ткани мозга.
НОРМАЛЬНЫЕ ВОЗРАСТНЫЕ ИЗМЕНЕНИЯ БЕЛОГО ВЕЩЕСТВА НА МРТ
К ожидаемым возрастным изменениям относятся:
- Перивентрикулярные «шапочки» и «полосы»
- Умеренно выраженная атрофия с расширением борозд и желудочков мозга
- Точечные (и иногда даже диффузные) нарушения нормального сигнала от мозговой ткани в глубоких отделах белого вещества (1-й и 2-й степени по шкале Fazekas)
Перивентрикулярные «шапочки» представляют собой области, дающие гиперинтенсивный сигнал, расположенные вокруг передних и задних рогов боковых желудочков, обусловленные побледнением миелина и расширением периваскулярных пространств. Перивентрикулярные «полосы» или «ободки» это тонкие участки линейной формы, расположенные параллельно телам боковых желудочков, обусловленные субэпендимальным глиозом.
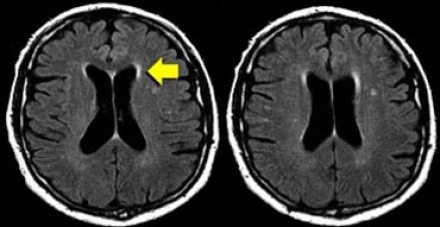
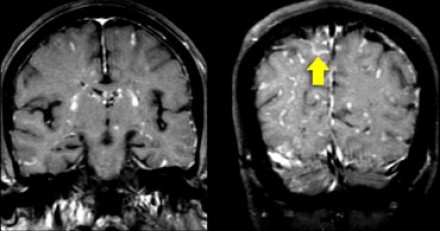
На магнитно-резонансных томограммах продемонстрирована нормальная возрастная картина: расширение борозд, перивентрикулярные «шапочки» (желтая стрелка), «полосы» и точечные очажки в глубоком белом веществе.
Клиническое значение возрастных изменений мозга недостаточно хорошо освещено. Тем не менее, имеется связь между очагами и некоторыми факторами риска возникновения цереброваскулярных расстройств. Одним из самых значительных факторов риска является гипертония, особенно, у пожилых людей.
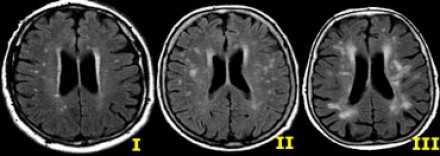
Степень вовлечения белого вещества в соответствии со шкалой Fazekas:
- Легкая степень – точечные участки, Fazekas 1
- Средняя степень – сливные участки, Fazekas 2 (изменения со стороны глубокого белого вещества могут расцениваться как возрастная норма)
- Тяжелая степень – выраженные сливные участки, Fazekas 3 (всегда являются патологическими)
ДИСЦИРКУЛЯТОРНАЯ ЭНЦЕФАЛОПАТИЯ НА МРТ
Очаговые изменения белого вещества сосудистого генеза — самая частая МРТ-находка у пациентов пожилого возраста. Они возникают в связи с нарушениями циркуляции крови по мелким сосудам, что является причиной хронических гипоксических/дистрофических процессов в мозговой ткани.
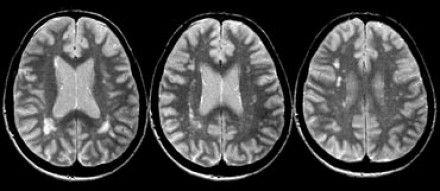
На серии МР-томограмм: множественные гиперинтенсивные участки в белом веществе головного мозга у пациента, страдающего гипертонической болезнью.
На МР-томограммах, представленных выше, визуализируются нарушения МР-сигнала в глубоких отделах больших полушарий. Важно отметить, что они не являются юкставентрикулярными, юкстакортикальными и не локализуются в области мозолистого тела. В отличие от рассеянного склероза, они не затрагивают желудочки мозга или кору. Учитывая, что вероятность развития гипоксически-ишемических поражений априори выше, можно сделать заключение о том, что представленные очаги, вероятнее, имеют сосудистое происхождение.
Только при наличии клинической симптоматики, непосредственно указывающей на воспалительное, инфекционное или иное заболевание, а также токсическую энцефалопатию, становится возможным рассматривать очаговые изменения белого вещества в связи с этими состояниями. Подозрение на рассеянный склероз у пациента с подобными нарушениями на МРТ, но без клинических признаков, признается необоснованным.
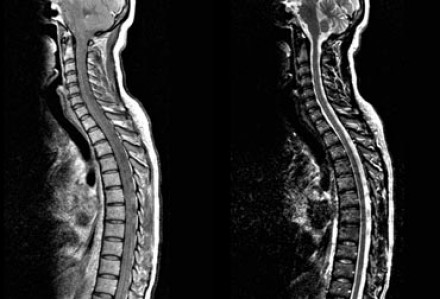
На представленных МР-томограммах патологических участков в спинном мозге не выявлено. У пациентов, страдающих васкулитами или ишемическими заболеваниями, спинной мозг обычно не изменен, в то время как у пациентов с рассеянным склерозом в более чем 90% случаев обнаруживаются патологические нарушения в спинном мозге. Если дифференциальная диагностика очагов сосудистого характера и рассеянного склероза затруднительна, например, у пожилых пациентов с подозрением на РС, может быть полезна МРТ спинного мозга.
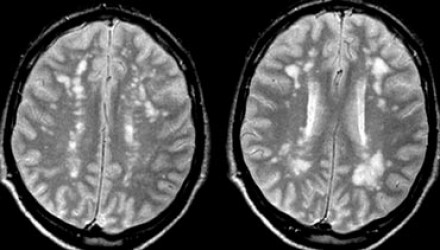
Вернемся снова к первому случаю: на МР-томограммах выявлены очаговые изменения, и сейчас они гораздо более очевидны. Имеет место распространенное вовлечение глубоких отделов полушарий, однако дугообразные волокна и мозолистое тело остаются интактными. Нарушения ишемического характера в белом веществе могут проявляться как лакунарные инфаркты, инфаркты пограничной зоны или диффузные гиперинтенсивные зоны в глубоком белом веществе.
Лакунарные инфаркты возникают в результате склероза артериол или мелких пенетерирующих медуллярных артерий. Инфаркты пограничной зоны возникают в результате атеросклероза более крупных сосудов, например, при каротидной обструкции или вследствие гипоперфузии.
Структурные нарушения артерий головного мозга по типу атеросклероза наблюдаются у 50% пациентов старше 50 лет. Они также могут обнаруживаться и у пациентов с нормальным артериальным давлением, однако более характерны для гипертоников.
САРКОИДОЗ ЦЕНТРАЛЬНОЙ НЕРВНОЙ СИСТЕМЫ
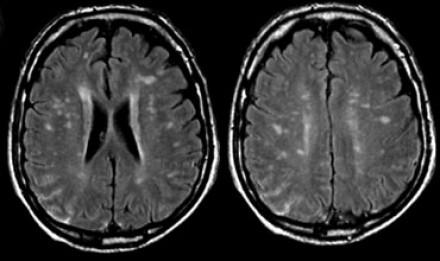
Распределение патологических участков на представленных МР-томограммах крайне напоминает рассеянный склероз. Помимо вовлечения глубокого белого вещества визуализируются юкстакортикальные очаги и даже «пальцы Доусона». В итоге было сделано заключение о саркоидозе. Саркоидоз не зря называют «великим имитатором», т. к. он превосходит даже нейросифилис по способности симулировать проявления других заболеваний.

На Т1 взвешенных томограммах с контрастным усилением препаратами гадолиния, выполненных этому же пациенту, что и в предыдущем случае, визуализируются точечные участки накопления контраста в базальных ядрах. Подобные участки наблюдаются при саркоидозе, а также могут быть обнаружены при системной красной волчанке и других васкулитах. Типичным для саркоидоза в этом случае считается лептоменингеальное контрастное усиление (желтая стрелка), которое происходит в результате гранулематозного воспаления мягкой и паутинной оболочки.
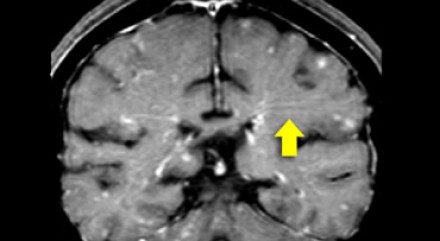
Еще одним типичным проявлением в этом же случае является линейное контрастное усиление (желтая стрелка). Оно возникает в результате воспаления вокруг пространств Вирхова-Робина, а также считается одной из форм лептоменингеального контрастного усиления. Таким образом объясняется, почему при саркоидозе патологические зоны имеют схожее распределение с рассеянным склерозом: в пространствах Вирхова-Робина проходят мелкие пенетрирующие вены, которые поражаются при РС.
БОЛЕЗНЬ ЛАЙМА (БОРРЕЛИОЗ)
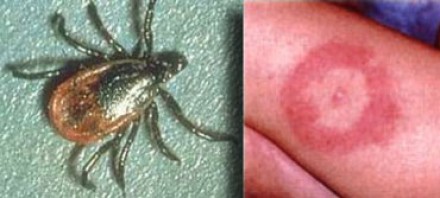
На фотографии справа: типичный вид сыпи на коже, возникающей при укусе клеща (слева) — переносчика спирохет.
Болезнь Лайма, или боррелиоз, вызывают спирохеты (Borrelia Burgdorferi), переносчиком инфекции являются клещи, заражение происходит трансмиссивным путем (при присасывании клеща). В первую очередь при боррелиозе на возникает кожная сыпь. Через несколько месяцев спирохеты могут инфицировать ЦНС, в результате чего появляются патологические участки в белом веществе, напоминающие таковые при рассеянном склерозе. Клинически болезнь Лайма проявляется острой симптоматикой со стороны ЦНС (в том числе, парезами и параличами), а в некоторых случаях может возникать поперечный миелит.
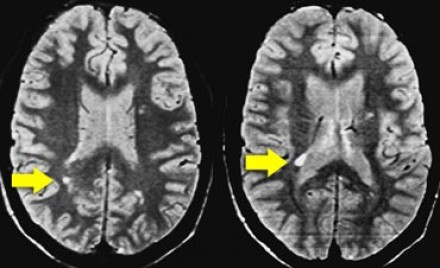
Ключевой признак болезни Лайма — это наличие мелких очажков размером 2-3 мм, симулирующих картину рассеянного склероза, у пациента с кожной сыпью и гриппоподобным синдромом. К другим признакам относится гиперинтенсивный сигнал от спинного мозга и контрастное усиление седьмой пары черепно-мозговых нервов (корневая входная зона).
ПРОГРЕССИРУЮЩАЯ МУЛЬТИФОКАЛЬНАЯ ЛЕЙКОЭНЦЕФАЛОПАТИЯ, ОБУСЛОВЛЕННАЯ ПРИЕМОМ НАТАЛИЗУМАБА
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) является демиелинизирующим заболеванием, обусловленным вирусом Джона Каннингема у пациентов с иммунодефицитом. Натализумаб представляет собой препарат моноклоанальных антител к интегрину альфа-4, одобренный для лечения рассеянного склероза, т. к. он оказывает положительный эффект клинически и при МРТ исследованиях.
Относительно редкий, но в то же время серьезный побочный эффект приема этого препарата — повышение риска развития ПМЛ. Диагноз ПМЛ основывается на клинических проявлениях, обнаружении ДНК вируса в ЦНС (в частности, в цереброспинальной жидкости), и на данных методов визуализации, в частности, МРТ.
По сравнению с пациентами, у которых ПМЛ обусловлен другими причинами, например, ВИЧ, изменения на МРТ при ПМЛ, связанной с приемом натализумаба, могут быть описаны как однородные и с наличием флюктуации.
Ключевые диагностические признаки при этой форме ПМЛ:
- Фокальные либо мультифокальные зоны в подкорковом белом веществе, расположенные супратенториально с вовлечением дугообразных волокон и серого вещества коры; менее часто поражается задняя черепная ямка и глубокое серое вещество
- Характеризуются гиперинтенсивным сигналом на Т2
- На Т1 участки могут быть гипо- или изоинтенсивными в зависимости от степени выраженности демиелинизации
- Примерно у 30% пациентов с ПМЛ очаговые изменения усиливаются при контрастировании. Высокая интенсивность сигнала на DWI, особенно по краю очагов, отражает активный инфекционный процесс и отек клеток
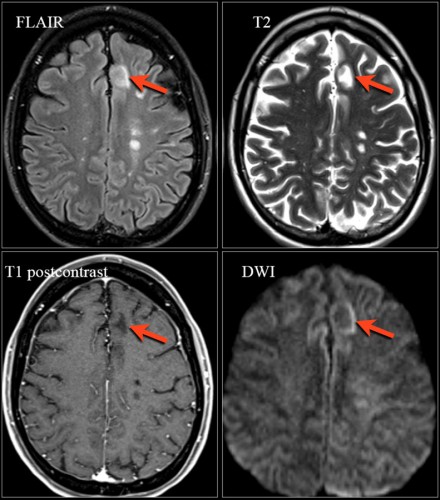
На МРТ видны признаки ПМЛ, обусловленной приемом натализумаба. Изображения любезно предоставлены Bénédicte Quivron, Ла-Лувьер, Бельгия.
Дифференциальная диагностика между прогрессирующим РС и ПМЛ, обусловленной приемом натализумаба, может быть достаточно сложной. Для натализумаб-ассоциированной ПМЛ характерны следующие нарушения:
- В выявлении изменений при ПМЛ наибольшей чувствительностью обладает FLAIR
- Т2-взвешенные последовательности позволяют визуализировать отдельные аспекты поражений при ПМЛ, например, микрокисты
- Т1 ВИ с контрастом и без него полезны для определения степени демиелинизации и обнаружения признаков воспаления
- DWI: для определения активной инфекции
Дифференциальная диагностика РС и ПМЛ
| Рассеянный склероз | ПМЛ | |
| Форма | Овоидная | Диффузные участки |
| Края | Четко очерченные | Расплывчатые, нечеткие |
| Размер | 3-5 мм | Больше 5 мм |
| Локализация | Перивентрикулярно («пальцы Доусона») | Субкортикальные отделы |
| Объемное воздействие | Присутствует при зонах большого размера | Отсутствует |
| Динамика в течение 1 месяца | Разрешение | Прогрессивное увеличение в размерах |
БЕЛОЕ ВЕЩЕСТВО ПРИ ВИЧ-ИНФЕКЦИИ
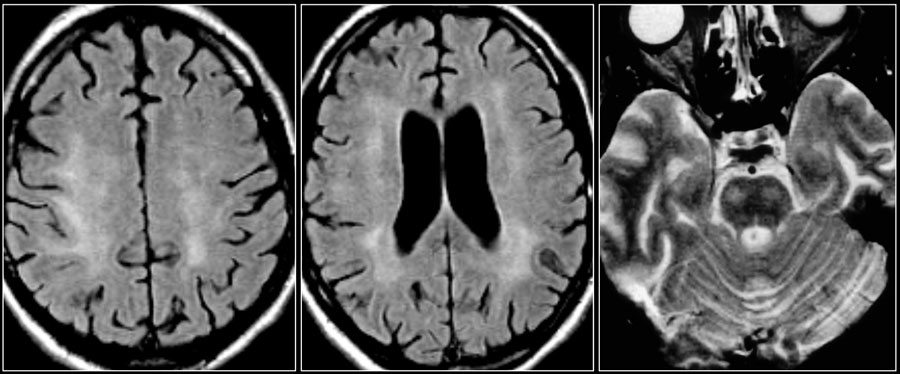
Ключевыми изменениями при ВИЧ-инфекции являются атрофия и симметричные перивентрикулярные или более диффузные зоны у пациентов со СПИДом.
Церебральная аутосомно-доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией (CADASIL)
Данное сосудистое заболевание считается врожденным и характеризуется следующими ключевыми клиническими признаками: мигренью, деменцией; а также отягощенной семейной историей. Характерными диагностическими находками являются субкортикальные лакунарные инфаркты с наличием мелких кистозных очажков и лейкоэнцефалопатии у подростков. Локализация поражения белого вещества в переднем полюсе лобной доли и в наружной капсуле признана высокоспецифичным признаком.
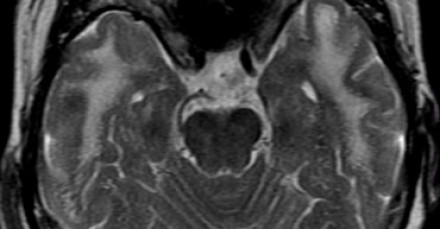
МРТ головного мозга при синдроме CADASIL. Характерное вовлечение височных долей.
Текст составлен на основе материалов сайта https://www.radiologyassistant.nl
Василий Вишняков, врач-радиолог
Читать подробнее о Втором мнении
Читать подробнее о телемедицине

Кандидат медицинских наук, член Европейского общества радиологов
Источник
Отек головного мозга — стремительно развивающееся накопление жидкости в церебральных тканях, без оказания адекватной медицинской помощи приводящее к смертельному исходу. Основу клинической картины составляет постепенно или быстро нарастающее ухудшение состояния больного и углубление расстройств сознания, сопровождающееся менингеальными знаками и мышечной атонией. Подтверждают диагноз данные МРТ или КТ головного мозга. Дополнительное обследование осуществляется для поиска причины отека. Терапия начинается с дегидратации и поддержания метаболизма церебральных тканей, сочетается с лечением причинного заболевания и назначением симптоматических препаратов. По показаниям возможно срочное (декомпрессионная трепанация, вентрикулостомия) или отсроченное (удаление объемного образования, шунтирование) хирургическое лечение.
Общие сведения
Набухание головного мозга было описано еще в 1865 году Н.И. Пироговым. На сегодняшний день стало понятно, что отек головного мозга не является самостоятельной нозологической единицей, а представляет собой вторично развивающийся патологический процесс, возникающий как осложнение целого ряда заболеваний. Следует отметить, что отек любых других тканей организма — достаточно часто встречающееся явление, совсем не относящееся к ургентным состояниям. В случае головного мозга, отек является жизнеугрожающим состоянием, поскольку, находясь в замкнутом пространстве черепа, церебральные ткани не имеют возможности увеличиваться в объеме и оказываются сдавленными. Вследствие полиэтиологичности отека мозга, в своей практике с ним сталкиваются как специалисты в области неврологии и нейрохирургии, так и травматологи, неонатологи, онкологи, токсикологи.
Отек головного мозга
Причины отека головного мозга
Наиболее часто отек головного мозга развивается при травмировании или органическом поражении его тканей. К таким состояниям относятся: тяжелая ЧМТ (ушиб головного мозга, перелом основания черепа, внутримозговая гематома, субдуральная гематома, диффузное аксональное повреждение, операции на головном мозге), обширный ишемический инсульт, геморрагический инсульт, субарахноидальное кровоизлияние и кровоизлияние в желудочки, первичные опухоли головного мозга (медуллобластома, гемангиобластома, астроцитома, глиома и др.) и его метастатическое поражение. Отек церебральных тканей возможен как осложнение инфекционных заболеваний (энцефалита, менингита) и гнойных процессов головного мозга (субдуральной эмпиемы).
Наряду с внутричерепными факторами к отеку мозга может привести анасарка, возникшая вследствие сердечной недостаточности, аллергические реакции (отек Квинке, анафилактический шок), острые инфекции (токсоплазмоз, скарлатина, свиной грипп, корь, паротит), эндогенные интоксикации (при тяжелом течении сахарного диабета, ОПН, печеночной недостаточности), отравления различными ядами и некоторыми медикаментами.
В отдельных случаях отек головного мозга наблюдается при алкоголизме, что связано с резко повышенной сосудистой проницаемостью. У новорожденных отек мозга бывает обусловлен тяжелым токсикозом беременной, внутричерепной родовой травмой, обвитием пуповиной, затяжными родами. Среди любителей высокогорного спорта встречается т. н. «горный» отек мозга, являющийся результатом слишком резкого набора высоты без необходимой акклиматизации.
Патогенез
Основным звеном в развитии церебрального отека выступают микроциркуляторные нарушения. Первоначально они, как правило, возникают в области очага поражения мозговой ткани (участка ишемии, воспаления, травмы, кровоизлияния, опухоли). Развивается локальный перифокальный отек головного мозга. В случаях тяжелого поражения головного мозга, не проведения своевременного лечения или отсутствия должного эффекта последнего, возникает расстройство сосудистой регуляции, ведущее к тотальному расширению церебральных сосудов и подъему внутрисосудистого гидростатического давления. В результате жидкая часть крови пропотевает через стенки сосудов и пропитывает церебральную ткань. Развивается генерализованный отек головного мозга и его набухание.
В описанном выше процессе ключевыми компонентами являются сосудистый, циркуляторный и тканевой. Сосудистым компонентом выступает повышенная проницаемость стенок мозговых сосудов, циркуляторным — артериальная гипертензия и расширение сосудов, которые приводят к многократному повышению давления в церебральных капиллярах. Тканевой фактор заключается в склонности тканей головного мозга при недостаточности кровоснабжения накапливать жидкость.
В ограниченном пространстве черепной коробки 80-85% объема приходится на церебральные ткани, от 5 до 15% — на цереброспинальную жидкость (ликвор), около 6% занимает кровь. У взрослого нормальное внутричерепное давление в горизонтальном положении варьирует в пределах 3-15 мм рт. ст. Во время чихания или кашля оно ненадолго поднимается до 50 мм рт. ст., что не вызывает расстройств функционирования ЦНС. Отек головного мозга сопровождается быстро нарастающим повышением внутричерепного давления за счет увеличения объема церебральных тканей. Происходит сдавление сосудов, что усугубляет микроциркуляторные нарушения и ишемию мозговых клеток. Вследствие метаболических нарушений, в первую очередь гипоксии, возникает массовая гибель нейронов.
Кроме того, резкая внутричерепная гипертензия может приводить к дислокации нижележащих церебральных структур и ущемлению ствола мозга в большом затылочном отверстии. Нарушение функции находящихся в стволе дыхательного, сердечно-сосудистого и терморегуляторного центров является причиной многих летальных исходов.
Классификация
В связи с особенностями патогенеза отек головного мозга подразделяется на 4 типа: вазогенный, цитотоксический, осмотический и интерстициальный. Самым часто встречающимся типом является вазогенный отек головного мозга, в основе которого лежит повышение проницаемости гематоэнцефалического барьера. В патогенезе основную роль играет переход жидкости из сосудов в белое мозговое вещество. Вазогенный отек возникает перифокально в зоне опухоли, абсцесса, ишемии, оперативного вмешательства и т. п.
Цитотоксический отек мозга является результатом дисфункции глиальных клеток и нарушений в осморегуляции мембран нейронов. Развивается преимущественно в сером мозговом веществе. Его причинами могут выступать: интоксикации (в т. ч. отравление цианидами и угарным газом), ишемический инсульт, гипоксия, вирусные инфекции.
Осмотический отек головного мозга возникает при повышении осмолярности церебральных тканей без нарушения работы гематоэнцефалического барьера. Возникает при гиперволемии, полидипсии, утоплении, метаболических энцефалопатиях, неадекватном гемодиализе. Интерстициальный отек появляется вокруг церебральных желудочков при пропотевании через их стенки жидкой части ликвора.
Симптомы отека головного мозга
Ведущим признаком отека мозга является расстройство сознания, которое может варьировать от легкого сопора до комы. Нарастание глубины нарушения сознания свидетельствует о прогрессировании отека. Возможно, что дебютом клинических проявлений будет потеря сознания, отличающаяся от обычного обморока своей длительностью. Зачастую прогрессирование отека сопровождается судорогами, которые через короткий промежуток времени сменяются мышечной атонией. При осмотре выявляются характерные для менингита оболочечные симптомы.
В случаях, когда отек головного мозга возникает на фоне хронической или постепенно развивающейся острой церебральной патологии, сознание больных в начальном периоде может быть сохранено. Тогда основной жалобой выступает интенсивная головная боль с тошнотой и рвотой, возможны двигательные нарушения, зрительные расстройства, дискоординация движений, дизартрия, галлюцинаторный синдром.
Грозными признаками, свидетельствующими о сдавлении ствола мозга, являются: парадоксальное дыхание (глубокие вдохи наряду с поверхностными, вариативность временных промежутков между вдохами), резкая артериальная гипотония, нестабильность пульса, гипертермия свыше 40°C. Наличие расходящегося косоглазия и «плавающих» глазных яблок говорит о разобщении подкорковых структур от коры головного мозга.
Диагностика отека мозга
Заподозрить отек мозга неврологу позволяет прогрессирующее ухудшение состояния пациента и нарастание нарушения сознания, сопровождающиеся менингеальными симптомами. Подтверждение диагноза возможно при помощи КТ или МРТ головного мозга. Проведение диагностической люмбальной пункции опасно дислокацией церебральных структур со сдавлением мозгового ствола в большом затылочном отверстии. Сбор анамнестических данных, оценка неврологического статуса, клинический и биохимический анализ крови, анализ результатов нейровизуализирующего исследования — позволяют сделать заключение относительно причины отека мозга.
Поскольку отек мозга является угрентным состоянием, требующим неотложной медицинской помощи, его первичная диагностика должна занимать минимум времени и проводиться в стационарных условиях на фоне лечебных мероприятий. В зависимости от ситуации она осуществляется в условиях реанимационного отделения или отделения интенсивной терапии.
Лечение отека головного мозга
Приоритетными направлениями в терапии отека мозга выступают: дегидратация, улучшение церебрального метаболизма, устранение первопричины отека и лечение сопутствующих симптомов. Дегидратационная терапия имеет целью выведение избытка жидкости из церебральных тканей. Она осуществляется путем внутривенных инфузий маннита или других осмотических диуретиков с последующим назначением петлевых диуретиков ( торасемида, фуросемида). Дополнительное введение 25% р-ра магния сульфата и 40% р-ра глюкозы потенцирует действие диуретиков и снабжает церебральные нейроны питательными веществами. Возможно применение L-лизина эсцината, который обладает способностью выводить жидкость, хотя и не является мочегонным препаратом.
С целью улучшения церебрального метаболизма проводится оксигенотерапия (при необходимости — ИВЛ), местная гипотермия головы, введение метаболитов (мексидола, кортексина, цитиколина). Для укрепления сосудистой стенки и стабилизации клеточных мембран применяют глюкокортикостероиды (преднизолон, гидрокортизон).
В зависимости от этиологии отека мозга в его комплексное лечение включают дезинтоксикационные мероприятия, антибиотикотерапию, удаление опухолей, ликвидацию гематом и участков травматического размозжения головного мозга, шунтирующие операции (вентрикулоперитонеальное дренирование, вентрикулоцистерностомию и др.). Этиотропное хирургическое лечение, как правило, проводят только на фоне стабилизации состояния пациента.
Симптоматическая терапия направлена на купирование отдельных проявлений заболевания, осуществляется путем назначения противорвотных средств, антиконвульсантов, обезболивающих препаратов и т. п. По показаниям в ургентном порядке с целью уменьшения внутричерепного давления нейрохирургом может быть проведена декомпрессивная трепанация черепа, наружное вентрикулярное дренирование, эндоскопическое удаление гематомы.
Прогноз
В начальной стадии отек мозга представляет собой обратимый процесс, по мере прогрессирования он приводит к необратимым изменениям мозговых структур — гибели нейронов и деструкции миелиновых волокон. Быстрое развитие указанных нарушений обуславливает то, что полностью ликвидировать отек с 100% восстановлением мозговых функций удается лишь при его токсическом генезе у молодых и здоровых пациентов, вовремя доставленных в специализированное отделение. Самостоятельная регрессия симптомов наблюдается лишь при горном отеке мо
