Толщина воротникового отека норма

ПРЕНАТАЛЬНЫЙ СКРИНИНГ I ТРИМЕСТРА БЕРЕМЕННОСТИ
Пренатальный скрининг первого триместра имеет большие возможности для выявления патологии в ранние сроки беременности, когда можно исключить не только анатомичесике аномалии, но и определить риски рождения больного ребенка.
Оптимальным сроком для проведения пренатального скрининга первого триместра (измерения толщины воротникового пространства, костей носа, оценки кровотока в венозном протоке, выявления трикуспидальной регургитации и др. является:
– срок беременности 11+0 – 13+6 недель,
– минимальная величина КТР плода составляет 45 мм,
– максимальная величина КТР плода не превышает 84 мм.
* КТР – копчико-теменного размер плода.
Ультразвуковой скрининг – в 11+0 -13+6 недель можно выявить ультразвуковые маркеры (признаки) хромосомной патологии плода – увеличение толщины воротникового пространства плода, отсутствие носовой кости, патологический кровоток в венозном протоке, наличие трикуспидальной регургитации (недостаточность трехстворчатого клапана сердца).
Толщина воротникового пространства (ТВП)
Воротниковое пространство является ультразвуковым проявлением скопления жидкости под кожей в тыльной области шеи плода в первом триместре беременности.
Толщина воротникового пространства в норме увеличивается во время беременности с увеличением копчико-теменного размера плода.
 |  |  |
ТВП в норме | Увеличение ТВП | Увеличение ТВП |
Во втором триместре беременности воротниковое пространство обычно исчезает или, в редких случаях, трансформируется или в отек шеи, или в кистозную гигрому в сочетании с генерализованным отеком плода или без такового.
Кости носа (НК)
Носовые кости в норме выявляются при УЗИ с 10 недели беременности. У плодов с хромосомной патологией процессы окостенения происходят позже, поэтому отсутствие костей носа или уменьшенные размеры в эти сроки могут быть признаком хромосомной патологии плода.
При ультразвуковом исследовании в 11-13+6 недель кости носа плода не визуализируются у 60-70% плодов при трисомии 21 и у 2% плодов при нормальном кариотипе.
 |  |  |
НК – норма | НК – норма | Патология-отсутствие НК |
Венозный проток (ВП)
Патологическая форма кривых скоростей кровотока в венозном протоке наблюдается у 80% плодов при трисомии 21 и у 5% плодов при нормальном кариотипе.
 |  |  |
№1 – ВП – норма | №2 – ВП – норма | № 3 – ВП – патология |
Патологический кровоток – нулевой или реверсный кровоток в венозном протоке рис. №3 (пики на – или – ниже изолинии). Нулевые и реверсные значения кровотока в ВП в фазу сокращения предсердий являются маркером ХА. Известно, что ХА часто сопровождаются врожденными пороками сердца, которые в ранние сроки беременности могут приводить к изменению кровотока в ВП. Патологический кровоток в ВП у плодов с нормальным кариотипом встречается не часто.
Tрикуспидальный клапан (ТК)
Трикуспидальная регургитация часто отмечается у плодов с ХА в ранние сроки беременности. ХА были обнаружены у 94,7% плодов с расширенным воротниковым пространством и изолированной трикуспидальной регургитацией в 11 -14 нед беременности. Описаны случаи изолированной трикуспидальной регургитации в 12-13 нед беременности у плодов, у которых в ходе пренатального кариотипирования была диагностирована трисомия 21. Также имеются сообщения о трикуспидальной регургитации в 11-14 нед у плодав с трисомией 21 и у плодов с трисомией 18, тогда, каку плодов с нормальным кариотипом -только в 0,7% случаев.
 |  |  |
№ 1 – ТК – норма | № 2 – ТК – патология | № 3 – ТК – патология |
Трикуспидальная регургитация рис. №2 и №3 – патология (ниже изолинии видны дополнительные сигналы, которые указывают обратный ток крови из правого желудочка в правое предсердие, при закрытых створках).
Обнаружение трикуспидальной регургитации в любом скроке беременности указывает на необходимость детального исследования сердца плода для исключения сердечной патологии.
Частота встречаемости других маркеров хромосомной патологии плода, таких, как омфалоцеле, мегацистис, единственная артерия пуповины и др. при определенных хромосомных заболеваниях выше, чем при нормальном кариотипе плода.
ВАЖНО
Основным маркером ХА (хромосомных аномалий) в ранние сроки беременности является расширение воротникового пространства плода. В случаях обнаружения этого маркера пренатальное кариотипирование является необходимым компонентом пренатального обследования в ранние сроки беременности.
Допплеровские технологии и оценку костей носа плода следует рассматривать важными дополнительными признаками, позволяющими повысить эффективность ранней пренатальной диагностики ХА, особенно в случаях пограничных или «спорных» расширений воротникового пространства.
В некоторых случаях оценка костей носа плода и обнаружение патологического кровотока в венозном протоке позволяет диагностировать ХА при нормальных значениях воротникового пространства.
В случаях, когда воротниковое пространство расширено, дополнительное обнаружение патологического кровотока в венозном протоке и отсутствие или гипоплазия костей носа плода, наличие трикуспидальной регургитации указывают на необходимость проведения пренатального кариотипирования (инвазивная диагностика).
Современный уровень развития медицинских технологий позволяет проводить обследование беременных женщин и выявление среди них группы риска по наличию болезни Дауна (трисомия 21) и других хромосомных болезней у плода уже начиная с 11 недель беременности. Наиболее эффективной признана комбинация ультразвукового и биохимического исследования в сроки 11 недель – 13 недель 6 дней.
БИОХИМИЧЕСКИЙ СКРИНИНГ крови беременной женщины позволяет определить концентрацию белков, вырабатывающихся в плаценте: РАРР-А и бета-ХГЧ. Для каждой недели беременности существуют собственные нормы содержания этих белков в крови, при хромосомной патологии плода соотношение белков будет меняться.
При трисомии 21 у плода в 12 недель беременности концентрация β-ХГЧ в сыворотке крови беременной женщины увеличена (около 2 МоМ) по сравнению с нормальными значениями для данного срока беременности, тогда как концентрация РАРР-А снижена (около 0,5 МоМ). При этом степень различия концентрации β-ХГЧ при трисомии 21 и при нормальном кариотипе увеличивается при увеличении срока беременности, тогда как степень различий в концентрации РАРР-А уменьшается. Эти временные изменения уровней биохимических маркеров и их зависимость от такого показателя, как вес беременной женщины, должны быть учтены при определении методики расчета определения индивидуального риска для конкретной пациентки.
Комбинация данных ультразвукового и биохимического исследования позволяет увеличить эффективность выявления плодов с болезнью Дауна до 85%. В настоящее время такой метод обследования является наиболее эффективным способом профилактики рождения ребенка с болезнью Дауна или другими хромосомными заболеваниями.
Для расчета риска хромосомных аномалий в нашем Центре используется программа
Astraia Software GmbH и ViewPoint GE Healthcare
Специалисты, занимающиеся расчетом риска хромосомной патологии плода на основании оценки его профиля, прошли соответствующее обучение и сертификацию (FMF), подтверждающую уровень качества выполнения данного вида ультразвукового исследования.
Более подробную информацию о специалистах с сертификатом компетентности FMF можно получить на официальном сайте FMF.
Сертификат FMF
/>
FMF – Fetal Medicine Foundation – (Фонд медицины плода) fetalmedicine.org – является зарегистрированной в Великобритании благотворительной организацией, которая организовала обучение и сертификацию специалистов по проведению ультразвукового скрининга в первом триместре беременности. Обучение включает в себя теоретический курс, практическое обучение стандартам получения ультразвуковых изображений и измерений ТВП, а также предоставление отчета по обучению, состоящего из ультразвуковых изображений проведенных исследований.
Оценка риска для трисомий />
ПРЕНАТАЛЬНАЯ ДИАГНОСТИКА
СКРИНИНГ I триместра. Комплексная диагностика в 11 нед. – 13 нед. беременности. Результаты готовы в день обращения!
Проводится оценка рисков:
– для трисомий 21, 18 и 13 на сроке беременности 11-13 недель путем сочетания материнского возраста + данных УЗИ – толщины воротникового пространства, частоты сердечных сокращений плода + исследования крови матери – материнской сыворотки ß-hCG и PAPP-A и расчетом риска на синдромы программой “ASTRAYA” с целью исключения патологии плода на этапе внутриутробного развития.
Комплексный подход в диагностике позволяет обнаружить плодов с высоким риском синдрома Дауна (трисомия 21); трисомии 18 ( синдрома Эдвардса); трисомии 13 (синдрома Патау), выявить нарушения развития внутренних органов плода, исключить пороки развития мозга, сердца и др. органов на ранних сроках.
В случае выявления у плода патологии, родителям предоставляется полная информация о характере и особенностях порока развития, возможностях современной медицины в плане реабилитации ребёнка. В результате семья принимает решение о судьбе данного ребёнка, тщательно взвесив свои собственные возможности.
Индивидуальный подход, интерпретация результатов, сопровождение на всех этапах УЗ- диагностики. Протокол исследования с комментарии (на любом иностранном языке) по желанию, высылаем по электронной почте.
– NEW! Дополнительно проводится оценка рисков
– риск преэклампсии;
– риск гестационного сахарного диабета;
– риск выкидыша на сроках 11-24 недели;
– риск мертворождения;
– риск ограничения (задержки) роста плода
– риск макросомии (вес плода при рождении более 4 кг);
– риск преждевременных родов ( – риск несостоятельности шейки матки ( ФЕТАЛЬНАЯ МЕДИЦИНА
Фетальная медицина – современный раздел акушерства, изучающий современные подходы к профилактике заболеваний плода, диагностике врожденных заболеваний, а также лечение некоторых угрожающих состояний непосредственно в утробе матери. Профилактическое направление позоляет определять риски рождения детей с врожденными пороками развития путем комлексной оценки результатов биохимических и инструментальных скринингов.
Ожидание малыша приносит будущей маме не только радость, но и различные страхи. И страх предстоящих родов – не самый сильный из них. По статистике, источником постоянных опасений становится здоровье еще не родившегося ребенка. «Как он там? Все ли с ним нормально?» – на эти вопросы отвечают скрининговые УЗ- исследования беременных, предназначенные для выявления возможных патологий на этапе внутриутробного развития будущего человека.
ИНВАЗИВНЫЕ МЕТОДЫ ДИАГНОСТИКИ
1. Биопсия хориона (10-12 недель) получение результатов (несколько дней); риск возможных осложнений 3-4%
2. Плацентоцентез (13-18 недель) получение результатов (несколько дней): риск возможных осложнений 3-4%
3. Амниоцентез (17-22 недели) получение результатов (несколько дней): риск возможных осложнений 0,5%
Источник
Гаврикова О.А., Чулков В.С., Брюхина Е.В.
Проблема наследственной и врожденной патологии, прежде всего врожденных пороков развития (ВПР), хромосомных и моногенных заболеваний за последнее десятилетие приобрела серьезную социально-медицинскую значимость. Частота врожденной и наследственной патологии в популяции составляет в среднем 5% от числа новорожденных детей. В структуре перинатальной заболеваемости и смертности врожденная и наследственная патология занимает 2-3 место. Широкое внедрение в клиническую практику скринингового ультразвукового исследования в 11-14 недель беременности позволяет провести раннюю пренатальную диагностику ВПР и хромосомных аномалий (ХА) [4]. Среди многочисленных эхографических маркеров ХА наиболее ценным считается толщина воротникового пространства [5]. Использование этого маркера позволяет выявлять до 66,7-92% хромосомных дефектов уже в ранние сроки беременности [6, 7]. Поэтому представляет научный интерес дальшейшее изучение увеличения толщины воротникового пространства (ТВП) плода как пренатального эхографического маркера врожденной и наследственной патологии.
Целью исследования явилась оценка величины толщины воротникового пространства плода в качестве маркера хромосомных аномалий и врожденных пороков развития плода.
Материал и методы. Тип исследования: когортное с проспективной когортой (2008 – 2010 г.).
Метод выборки: сплошной по мере обращения.
Критерии включения:
1. Беременность в сроке гестации 11-14 недель.
2. Известная дата последней менструации при 26-30 дневном цикле.
3. Согласие женщины на участие в исследовании.
Критерии исключения:
1. Нарушения менструального цикла.
2. Указание на прием гормональных контрацептивов за два месяца до цикла зачатия.
3. Стимулированная беременность.
4. Многоплодная беременность.
В соответствии с критериями включения/исключения за указанный период было отобрано 1310 беременных в сроки гестации от 11 до 14 недель, состоявших на диспансерном учете в женских консультациях г. Челябинска.
После проведения ультразвукового скрининга беременные были распределены на две группы, с учетом размеров толщины воротникового пространства (ТВП) плода: основная группа – 175 женщин с увеличением размеров толщины воротникового пространства у плода (группа 1), группа сравнения – 1135 пациенток с нормальными размерами толщины воротникового пространства у плода, беременность которых завершилась своевременными родами и рождением нормальных здоровых детей (группа 2). В качестве пороговых (разделительных) значений принимался 95‰ ТВП от показателей, разработанных в результате наших исследований, согласно рекомендациям Н.А. Алтынник и М.В. Медведева и К. Николаидеса и соавт. [1,7]. Группы были сопоставимы по возрасту, паритету и сроку гестации.
Эхографические исследования проведены на ультразвуковых сканерах фирмы TOSHIBA (Япония) высокого (XARIO XG) и экспертного (APLIO XG) классов. Для измерения размеров ТВП использовали трансабдоминальный доступ сканирования. В случаях регистрации у плода эхографических маркеров хромосомных дефектов или врожденных пороков развития, исследование завершали трансвагинальным доступом для детального изучения анатомии и проведения расширенной эхокардиографии плода. В ходе пренатального консультирования пациентке сообщали о наличии риска хромосомной патологии и объясняли целесообразность пренатального кариотипирования. В сроке 11-13 недель гестации осуществляли трансабдоминальную аспирацию ворсин хориона. При отказе от пренатального кариотипирования в ранние сроки и выявлении других эхографических маркеров хромосомной патологии или врожденных пороков развития плода во втором триместре беременности, рекомендовалась оценка кариотипа плода методом кордоцентеза в 21-24 недели.
Статистический анализ данных проводился при помощи пакета статистических программ ISTICA 6.0 (Soft, 2001) и программы MedCalc (9.1.0.1) for Windows. При распределении признака в выборке, близком к нормальному, количественные значения представлялись в виде средней арифметической и ее среднеквадратичного отклонения (M±σ).
Для оценки различий между двумя группами в количественных признаках с учетом характера распределения, близкому к нормальному, применяли t-критерий Стьюдента. Оценка межгрупповых различий по качественным признакам проводилась с использованием критерия χ2, а при ожидаемых частотах менее 10 – применялась поправка Йетса.
С целью оценки прогностической значимости показателей проводился ROC-анализ с вычислением чувствительности, специфичности, отношения положительного и отрицательного правдоподобия. Для всех видов анализа статистически достоверными считались значения p<0,05.
Результаты исследования. Возраст беременных варьировал от 16 до 45 лет. Средний возраст пациенток в группах оказался сопоставимым: в группе 1- 28,7±5,43 лет, в группе 2 – 29,0±6,10 лет (р>0,05).
Согласно полученных нами данным толщина воротникового пространства плода в группе 2 (со своевременными родами и рождением здорового ребенка) постепенно увеличивается на сроках от 11 до 14 недель, составляя в среднем 1,3±0,3 мм в 11-12 недель, 1,4±0,4 мм в 12-13 недель и 1,5±0,3 мм в 13-14 недель, при отсутствии различий между величинами ТВП в эти сроки беременности (р>0,05).
В табл. 1 представлены значения толщины воротникового пространства плода в 11-14 недель беременности в группах сравнения.
Таблица 1. Показатели толщины воротникового пространства плода в 11-14 недель беременности в группах сравнения
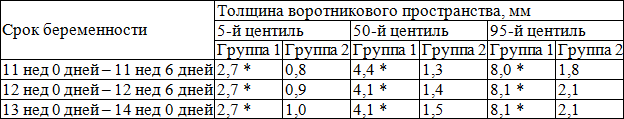
Примечание: * – значимость различий (р<0,05) при сравнении групп 1 и 2
В основной группе численные значения расширенного воротникового пространства плода варьировали от 2,5 до 11,0 мм и превышали соответствующие показатели (5-й, 50-й, 95-й центиль) в группе сравнения в 11-12, 12-13 и 13-14 недель беременности (рис. 1).
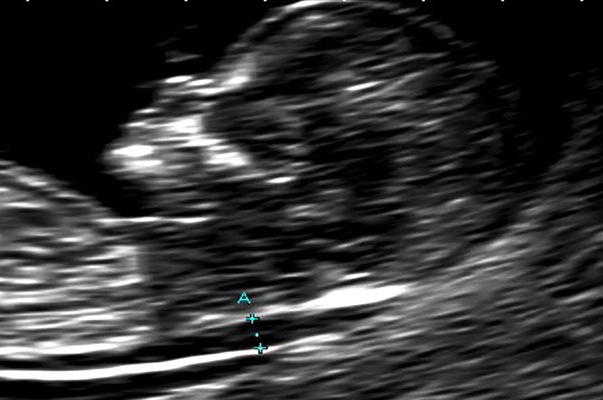
Рис. 1. Увеличение толщины воротникового пространства
Из 175 плодов, у которых в сроке 11-14 недель беременности было выявлено расширение воротникового пространства, пренатальное или постнатальное кариотипирование для исключения хромосомных аномалий было осуществлено в 160 случаях. Из них хромосомные дефекты были обнаружены в 46/160 (28,8%) наблюдениях. У 114/160 женщин (71,2%) кариотип был нормальным. В 15 случаях хромосомный набор плода/новорожденного остался за пределами наших знаний из-за отказа пациентки от инвазивной диагностической процедуры или из-за отсутствия достаточного количества метафаз в биоптате хориона.
Структура хромосомных аномалий представлена на рис. 2.
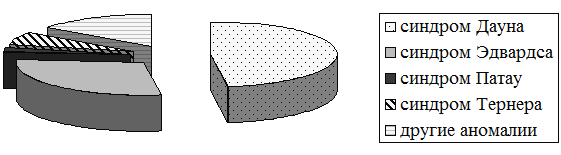
Рис. 2. Структура хромосомных аномалий у плодов
Среди диагностированных хромосомных аномалий наиболее часто встречались анэуплоидии (78,3%, n=22): синдром Дауна был зарегистрирован практически в каждом втором наблюдении (47,8%, n=22); почти в каждом третьем случае был выявлен синдром Эдвардса (28,3%, n=13), а синдром Патау, в нашем исследовании, явился самой редкой находкой (2,2%, n=1). Доля моносомии Х (синдром Тернера) составила 6,5% (n=3). Удельный вес других хромосомных дефектов составил 15,2% (n=7). Среди данных ХА регистрировались: триплоидии по Х-хромосоме (4,3%, n=2), несбалансированные транслокации (4,3%, n=2), патологические структурные изменения хромосом (2,2%, n=1), маркерные хромосомы (2,2%, n=1) и синдром анэуплоидии по половым хромсомам (2,2%, n=1).
Частота хромосомных аномалий варьировала в зависимости от величины толщины воротникового пространства, представлена на рис. 3.
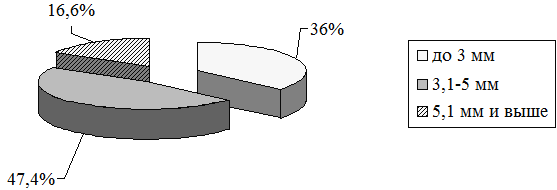
Рис. 3. Частота хромосомных аномалий варьировала в зависимости от величины толщины воротникового пространства
Таким образом, при увеличении численных значений ТВП возрастала частота хромосомных заболеваний.
Помимо этого, при регистрации расширения воротникового пространства практически в каждом втором случае (43,2%, n=76) обнаруживались врожденные пороки: их частота оказалась выше при аномального кариотипе, по сравнению с нормальным – 69,7% (n=53) и 30,3% (n=23) соответственно, р<0,001. Структура врожденных пороков развития в основной группе представлена в табл. 2.
При выявлении хромосомных аномалий в группе с расширением ТВП чаще диагностировались множественные пороки развития и врожденные пороки сердца, несколько реже встречались пороки ЖКТ, МПС, ЦНС, КМС и КГ шеи, по сравнению с таковыми у плодов/новорожденных с нормальным набором хромосом. Различий по частоте других пороков развития плода не выявлено.
Таблица 2. Структура врожденных пороков развития в группе с расширением ТВП в зависимости от кариотипа плода
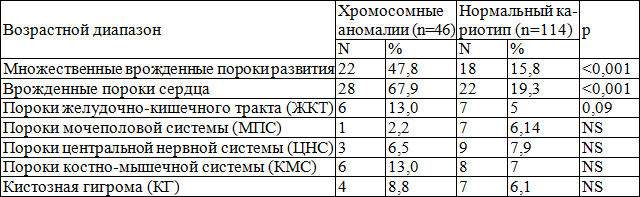
Примечание: NS – р>0,05
Таким образом, в соответствии с полученными данными, необходимо выделять пациенток с расширением ТВП у плода в группу высокого риска по врожденным порокам развития даже при отсутствии хромосомной патологии. Особое внимание следует уделять детальному изучению анатомии плода и эхокардиографическому исследованию, так как множественные врожденные пороки развития и пороки сердца регистрируются наиболее часто.
С целью оценки прогностического значения величины ТВП в отношении развития хромосомных аномалий плода в группах сравнения нами использовался ROC-анализ (рис. 4).
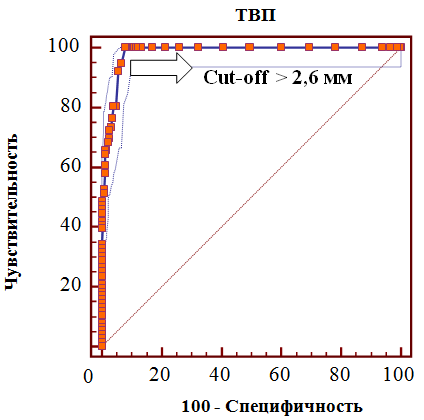
Рис. 4. ROC-кривая прогностического значения толщины воротникового пространства в отношении хромосомных аномалий плода
Проведенный анализ показал, что толщина воротникового пространства выше 2,6 мм ассоциирована с высоким риском развития хромосомных аномалий, причем указанный уровень имеет высокую чувствительность (100%) и специфичность (89,7%), а также отношение правдоподобия положительного результата (9,65), р<0,001.
В последние годы многими авторами были опубликованы сведения о том, что увеличение ТВП может отмечаться не только при хромосомной патологии у плода, но и при различных ВПР [2, 3]. Большинство из этих пороков, потенциально, могут быть диагностированы только в более поздние сроки беременности или даже после родов. С целью оценки прогностического значения величины ТВП в отношении врожденных пороков развития плода нами также использовался ROC-анализ (рис. 5). Оценка ассоциации ТВП с различными ВПР плода представлена в табл. 3.
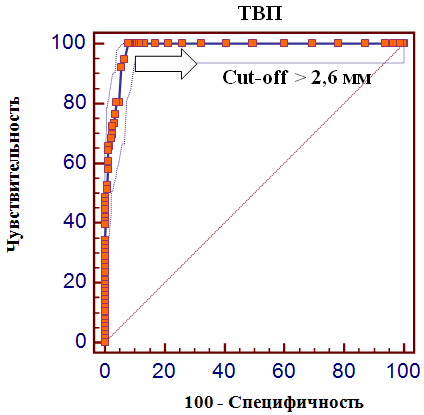
Рис. 5. ROC-кривая прогностического значения толщины воротникового пространства в отношении врожденных пороков развития плода
Согласно полученным данным, величина ТПВ выше 2,6-2,8 мм ассоциирована практически со всеми врожденными пороками развития, обладает высокой чувствительностью (100%) и специфичностью (87% и выше), что целесообразно использовать в клинической практике.
Выводы
1. В группе беременных с увеличением толщины воротникового пространства плода чаще встречаются хромосомные аномалии и врожденные пороки развития.
2. Толщина воротникового пространства выше 2,6 мм ассоциирована с высоким риском развития хромосомных аномалий (чувствительность – 100%, специфичность – 89,7%, отношение правдоподобия положительного результата – 9,65, р<0,001).
3. Толщина воротникового пространства выше 2,6-2,8 мм ассоциирована практически со всеми врожденными пороками плода (множественные врожденные пороки, врожденные пороки сердца, пороки желудочно-кишечного тракта и др.), обладая высокой чувствительностью (100%) и специфичностью (87% и выше).
4. Пороговые значения толщины воротникового пространства выше 2,6 мм целесообразно использовать в пренатальной диагностике врожденной патологии плода.
Таблица 3. Ассоциация толщины воротникового пространства с различными врожденными пороками развития по результатам ROC-анализа
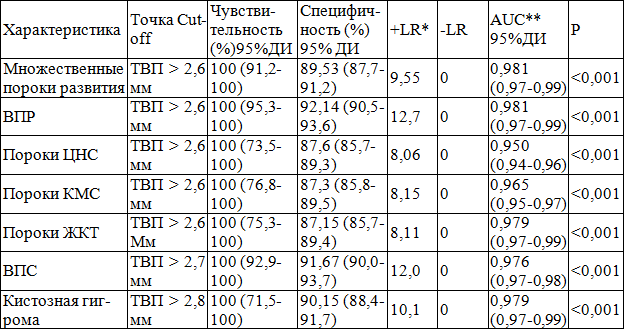
Примечания: * – + LR – положительное отношение правдоподобия; – LR – отрицательное отношение правдоподобия; AUC – площадь под ROC-кривой
Источник
