Режимы ивл при отеке легких
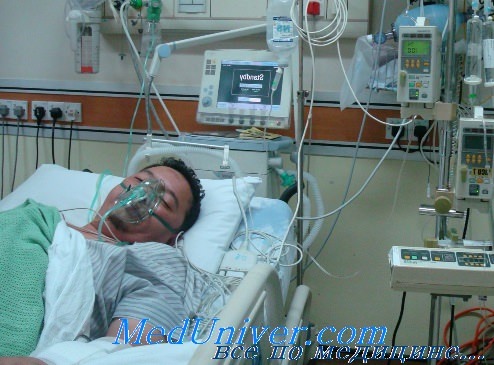
Искусственная вентиляция при отеке легких.
При неэффективности выше перечисленных мер и при быстро нарастающей гипоксии и гиперкапнии необходимо проведение интубации трахеи и ИВЛ.
Интубацрпо трахеи выполняют на фоне седации бензодиазепинами (мидазолам, диазепам) после предварительного орошения слизистой оболочки верхних дыхательных путей местным анестетиком (10% аэрозоль лидокаина).
ИВЛ при отеке легких проводят в режиме ПДКВ до +8 -+10 см Н2О. Устанавливать ПДКВ более 15 см H2O нецелесообразно, т. к. в этом случае возрастающее давление в альвеолах может вызывать “блок” кровотока в результате сдавления капилляров легких. Вентиляция проводится 100% кислородом, соотношение вдох/выдох – 1:1. МОД устанавливается до 20 л, частота дыхания – 22-24 в мршуту.
Аспирировать пену из дыхательных путей не следует, т. к. эта манипуляция усиливает отек.
Положительные эффекты ИВЛ в режиме ПДКВ при кардиогенном отеке связаны со снижением притока крови в венозный отдел карилляров легких в результате повышения внутриплеврального и внутриальвеолярного давления, с увеличением оксигенации гемоглобина крови вследствие увеличения диффузии кислорода через альвеолярно-капиллярную мембрану на фоне повышения парциального давления кислорода в альвеолах, с улучшением рши нормализацией вентиляционно-перфузионных отношений в легких, с возможностью активной регуляции уровня углекислого газа в крови на этапах, пока диффузионная способность альвеолярно-капиллярной мембраны для углекислого газа остается в пределах нормы.
Показанием для уменьшения ПДКВ являются снижению ЦВД и растяжимости легких при стабильных параметрах ИВЛ, что указывает на регресс отека лептах.

В ряде случаев при отсутствии возможности интубации трахеи и проведешь ИВЛ дыхание осуществляют в режрше непрерывного положительного давления в дыхательных путях.
Непрерывное положительное давление в дыхательных путях проводится при помощи прозрачного полиэтршенового мешка, надетого на голову больного и герметизируемого вокруг шеи поролоновой лентой. По углам мешка делают отверстия, в которые герметично закрепляют трубки для вдоха и выдоха. Трубка для вдоха присоединяется к источнику увлажненного кислорода рши воздушно-кислородной смеси, а трубка для выдоха опускается в воду на глубину 6-10 см. Это pi будет той величиной давления, которая обеспечивает постоянное положрггельное давление в дыхательных путях. Газоток устанавливается таким образом, чтобы мешок на голове больного постоянно находился в расправленном состоянии, а пузырьки газа в воде появлялись только во время выдоха.
Этот метод позволяет улучшить диффузию газов через альвеолярно-капиллярную мембрану, расправить микроателектазы, увеличить диффузионную поверхность легких, усилить элиминацию из организма углекислоты.
Дискутабельным остается вопрос о целесообразности включения в комплекс интенсивной терапии сердечных гликозидов. С нашей точки зрения улучшения сократимости миокарда при острой сердечной недостаточности не происходит: положительный эффект гликозидов в полной мере не развивается, периферическая вазоконстрикция способствует дальнейшему снижению сердечного выброса, терапевтический эффект развивается относительно медленно, аритмогенное действие гликозидов, потенцируемое гипоксией и гиперкатехолемией, общеизвестно.
Показанием для введения сердечных гликозидов является тахисистолическая форма мерцания или трепетания предсердий при застойной левожелудочковой недостаточности.
Назначение адренергических препаратов (допамин, добутамин) показано при остром отеке легких, вызванном снижением сократимости миокарда левого желудочка. При отеке легких, вызванном препятствием или блокадой кровотока (стеноз митрального отверстая, миксома или тромб левого предсердия, стеноз аортального отверстия), адренергические средства не используются, т. к. при их введении одновременно с усилением сократимости миокарда левого желудочка усиливается сократимость миокарда правого желудочка.
При остром кардиогенном отеке тахикардия усугубляет его развитие т. к. нарастающая тахикардия (до 110-130 уд./мин) вызывает возрастание минутного объема кровообращения. При более высокой тахикардии (более 135-150 уд./мин) возникает синдром “незавершенной” или “неполной” диастолы. В этом случае из-за снижения сердечного выброса отток крови из легочных вен уменьшается, давление в венозном отделе капилляра повышается. Поэтому целесообразно при тахикардии свыше 120 ул./мин для снижения частоты сердечных сокращений ввести внутривенно лидокаин в дозе 80-120 мг. При необходимости и по показаниям могут быть использованы и другие антиаритмические препараты.
Назначение атропина показано лишь в случае возникновения брадикардии, вызывающей опасные изменения (артериальную гипотензию).
Лечебная тактика при купировании кардиогенного отека легких во многом определяется состоянием гемодинамики и, в первую очередь, уровнем артериального давления. Особенности терапии отека легких при артериальной нормо-, гипер- и гипотензии представлены в таблице.
В заключение необходимо отметить, что тактика интенсивной терапии острого кардиогенного отека легких зависит от этапа и скорости его развития. Ключевым моментом в изменении тактики лечения острого кардиогенного отека легких является решение о переводе больного на ИВЛ. При изменении тактики необходимо учитывать, что гипердинамия сердечно-сосудистой системы, увеличение потребности организма к кислороде, отрицательное давление в альвеолах, дыхательная недостаточность создают “порочный круг”. Поэтому чем раньше удается его “разорвать”, тем более благоприятен прогноз.
– Также рекомендуем “Кардиогенный шок. Патофизиология кардиогенного шока.”
Оглавление темы “Кардиогенный шок. Искусственная вентиляция легких.”:
1. Интенсивная терапия кардиогенного отека легких.
2. Искусственная вентиляция при отеке легких.
3. Кардиогенный шок. Патофизиология кардиогенного шока.
4. Клиника кардиогенного шока. Интенсивная терапия кардиогенного шока.
5. Внутриаортальная баллонная контрпульсация. Искусственная вентиляция легких в реаниматологии.
6. Отношение времени вдоха и выдоха при вентиляции легких.
7. Традиционная искусственная вентиляции легких. ИВЛ с положительным давлением в конце выдоха.
8. ИВЛ с ограниченным Ppeak. ИВЛ с периодическим раздуванием легких. ИВЛ с управляемым давлением и инверсированным отношением вдох/выдох.
9. Чрескожная струйная ВЧ ИВЛ. Адаптация респиратора к больному.
10. Отключение больного от респиратора. Уход за больными, находящимися на ИВЛ.
Источник
В ситуации, когда у больного присутствует острая дыхательная недостаточность и в альвеолах легких скапливается жидкость, то есть происходит отек, крайне важно обеспечить поступление кислорода. Зачастую состояние пациента тяжелое и для проведения реанимационных мероприятий требуется его подключение к системе искусственной вентиляции. Она помогает поддерживать жизнь пациента, устраняет отек и позволяет выиграть время для проведения других лечебных мероприятий.
При отеке искусственная вентиляция легких используется в режиме положительного давления в конце выдоха (ПДКВ). Это позволяет увеличить внутрилегочное давление, снизить полнокровие и улучшить растяжимость легких. Однако данный режим не снижает количество внесосудистой жидкости и даже может увеличить ее, однако положительно влияет на расположение воды, вследствие чего улучшается газообмен.
Интубация трахеи проводится при помощи оксибутирата натрия или седуксена, также используются миорелаксин или дитилин. Далее, если показатели артериального давления выше 60 мм рт. ст. используется вентиляция легких с ПДКВ 8–10 см вод. ст. При этом пена из дыхательных путей не отсасывается, а ИВЛ устанавливается в режиме повышенного минутного объема дыхания до 20 л/мин и частотой до 24 циклов в минуту. После того как отек легкого купирован и состояние больного улучшилось эти параметры снижают.
Использование ИВЛ в режиме ПДКВ способствует уменьшению хрипов и улучшает проходимость дыхательных путей уже после нескольких циклов. Однако это не означает, что отек легких исчез. Поспешное снижение положительного давления или его отмена чаще всего приводят к ухудшению состояния больного и повторному образованию пены в легких. Чтобы судить о его ликвидации, помимо аскульатативных данных, необходимо учитывать показатели центрального венозного давления пациента. Если уменьшение ПДКВ не приводит к его снижению, то отключать сопротивление выдоху еще рано. Не менее важным показателем при отеке легких является эффективная растяжимость дыхательной системы. Если растяжимость при изначальных параметрах возрастает, то можно говорить о регрессе и ликвидации отека.
Показания к применению ИВЛ при отеке легких
Подключение больного к системе искусственной вентиляции при отеке легких может осуществляться по абсолютным или относительным показаниям.
Ситуации, требующие незамедлительного проведения ИВЛ:
- Продолжительная остановка дыхания.
- Прогрессирующие нарушения сознания и психики, обусловленные нарастающей гипоксией.
В таких случаях искусственная вентиляция жизненно важна, она позволяет поддерживать жизнь пациента и спасает его от умирания.
Относительные показания к использованию ИВЛ:
- Нарастающее истощение пациента на фоне «надрывного» дыхания.
- Цианоз, потливость, землистый цвет кожи.
- Повышенная работа дыхательных мышц, учащенное дыхание до 40 циклов в минуту, не исчезающее после снижения температуры.
- Выраженная тахикардия, брадикардия, неустойчивое артериальное давление, показатели парадоксального пульса выше 20 мм. рт. ст.
- Показатель артериального РО2 ниже 60 мм. рт. ст. при дыхании атмосферным воздухом, и ниже 70 мм. рт. ст. при кислородном.
Данные показания очень часто переходят в абсолютные, и поэтому при их появлении медлить с подключением больного к системе ИВЛ не следует. Даже если на тот момент проведение искусственной вентиляции легких не требуется для спасения жизни больного, она является единственно надежным и эффективным методом борьбы с острой дыхательной недостаточностью.
Зачастую в некритических ситуациях при отеке легких используется высокочастотная вспомогательная вентиляция, а подключение больного к системе ИВЛ с ПДКВ осуществляется при неэффективности других лечебных мероприятий. Последний метод позволяет достаточно быстро стабилизировать состояние больного и перед экстубацией трахеи его снова переводят на вспомогательную вентиляцию с поддержкой давлением.
Источник
Режимы искусственной вентиляции легких (ИВЛ): принудительный и вспомогательныйПринципиальным физиологическим эффектом искусственной вентиляции легких, в отличие от акта самостоятельного дыхания, является положительное давление в дыхательных путях во время дыхательного цикла. Положительное давление имеет ряд преимуществ при газообмене, включая рекрутинг периферических альвеол, увеличение функциональной остаточной емкости, улучшение вентиляционно-перфузионного соотношения и снижение внутрилегочного шунтирования крови. Отрицательные же эффекты заключаются в возможности появления баротравмы и респираторного повреждения легких при использовании больших дыхательных объемов или давления на вдохе, а также потенциальном снижении сердечного выброса при увеличении среднего внутригрудного давления. В общем, некоторая степень позитивных и негативных эффектов искусственной вентиляции легких свойственна всем используемым режимам. Эта величина неодинакова у различных режимов, что обусловлено уровнем положительного давления на вдохе. Принудительные (Control-mode, CV) и вспомогательные (assist/control-mode ventilation, ACV) режимы представляют собой циклические, объемные режимы, доставляющие фиксированный дыхательный объем с установленным минимальным числом вдохов и скоростью дыхательного потока. Дыхательные попытки пациента при первом варианте не являются триггерами для начала аппаратного вдоха. При CV, вентилятор не добавляет вдохов, несмотря на попытки пациента. Учитывая безопасность и комфорт вспомогательных режимов вентиляции, CV не должен применяться рутинно. Режим ACV позволяет по запросу больного в виде дыхательных попыток, инициировать дополнительный аппаратный вдох. В зависимости от состояния пациента, а также чувствительности и типа (потоковый или по давлению) триггера вдоха, режим позволяет пациенту создавать свой ритм дыхания и дыхательный объем (с установлением минимального количества вдохов в качестве системы защиты). Использование ACV типично у больных с паралитическими состояниями (при использовании мышечных релаксантов или при паралитических нейромышечных заболеваниях), требующих большого количества седативных средств, а также при трудностях с синхронизацией или при невозможности инициировать вдох в PSV или IMV режимах. Путем повышения аппаратной ЧДД, приводящего к снижению количества спонтанных вдохов, с помощью ACV режима можно добиться уменьшения работы дыхания пациента. Чрезмерное увеличение количества инициированных вдохов значительно увеличивает цену дыхания. С другой стороны триггер вдоха должен быть достаточно чувствительным, чтобы не приводить к возникновению избыточных усилий при дыхательных попытках, что быстро истощает больного. Режим вентиляции с контролем по объему (PRVC). При этом режиме возможно ограничение чрезмерно высокого пикового давления, приводящего к перерастяжению альвеол. При PCVR создается регулируемый, снижающийся поток на вдохе, который ограничивает пиковое давление, но доставляет установленный объем, в отличие от режима контроля вентиляции по давлению. Стоит отметить, что теоретические преимущества PCVR, не подтвердились рандомизированными исследованиями благоприятного эффекта при данном режиме, за исключением снижения пикового давления. Перемежающая принудительная вентиляция (IMV). Режим IMV был разработан в 1970-х с целью сохранения спонтанного дыхания пациента в дополнение к аппаратному, с заранее заданной минимальной частотой и объемом вдохов. Вначале данный режим использовался для отлучения пациента от вентилятора, обеспечивая плавный переход по сравнению с классическим методом использования Т-переходников. Синхронизированный вариант режима (SIMV) создавался для предотвращения наложения аппаратных вдохов на пик или окончание спонтанного вдоха пациента. SIMV продолжает широко использоваться как режим отлучения, и имеет преимущество, выражающееся в ступенчатом снижении частоты аппаратных вдохов и увеличении спонтанных. У пациентов со сниженным комплаенсом, IMV может не обеспечивать достаточный объем спонтанного вдоха из-за сильно ограниченных дыхательных возможностей. В данных условиях поддержка по давлению может быть использована в помощь к каждому вдоху IMV, значительно увеличивая объем спонтанного вдоха и снижая работу дыхания.
Вентиляция с поддержкой по давлению (PCV). Режим PSV был разработан в 1980-х как вспомогательный режим вентиляции. Каждый вдох в режиме PSV инициируется дышащим пациентом и поддерживается давлением, с максимальным потоком во время фазы вдоха. Окончание поддержки вдоха происходит в момент ослабления собственного потока вдоха пациента ниже установленного уровня, инициируя спонтанный выдох. В этом заключается отличие принципа переключения фаз вдох-выдох, регулируемого по потоку, от регуляции этого переключения по объему (рис. 60-3). Режим поддержки по давлению не подразумевает заранее установленной частоты аппаратных дыханий, так как каждый вдох должен быть инициирован пациентом. Это делает применение PSV невозможным у пациентов с нейромышечными заболеваниями, при применении мышечных релаксантов и глубокой седации. PSV присущи некоторые преимущества, включая улучшение синхронизации пациента с аппаратом ИВЛ, так как ритм дыхания задает сам больной. PSV может обеспечивать минимальную поддержку дыхания перед моментом эксту-бации или значительную (20-40 мм водн. ст.), что означает полное протезирование дыхательной функции пациента и минимальную работу дыхания. Как режим отлучения, поддержка по давлению может использоваться совместно с IMV режимом, как описано выше, или как единственный режим, с постепенным снижением давления поддержки, позволяя пациенту брать на себя больше работы по обеспечению дыхания. У пациентов со сниженными дыхательными резервами, заниженные уровни поддержки давлением могут приводить к неадекватному минутному объему дыхания, что требует постоянного мониторинга частоты и объема дыхания. Вентиляция с переключением фаз вдох-выдохВентиляция с переключением фаз вдох-выдох по объему в условиях тяжелого острого респираторного дистресс синдрома (ОРДС) и сниженного легочного комплаенса, может приводит к чрезмерному пиковому давлению или/и высокому объему вдоха в некоторых легочных сегментах, вызвав вторичное респиратор-ассоциированное легочное повреждение. Эти соображения привели к большему использованию режимов вентиляции с переключением фаз вдох-выдох по времени с регулированием по давлению. В этом режиме вентиляции дыхательный объем доставляется с постоянным потоком вплоть до достижения установленного давления. Время аппаратного вдоха устанавливается заранее и не зависит от потока, как в случае вентиляции с контролем по давлению. Контроль по давлению имеет преимущества в виде постоянного ограничения пикового давления, независимо от изменений податливости легких и грудной клетки или десинхронизации с аппаратом ИВЛ. Учитывая вышесказанное, это наиболее распространенный и безопасный режим вентиляции в условиях поражения легких, сопровождающихся низкой податливостью, что типично для ОРДС. Как бы то ни было, PCV не очень хорошо переносится пациентами в сознании, что часто требует достаточного уровня седации. Вентиляция с измененным соотношением фаз дыхания (IRV) может быть вариантом вентиляции с контролем по объему или по давлению, но наиболее часто используется при PCV. IRV является современной адаптацией практики прошлого, заключавшейся в удлинении фазы вдоха, результатом чего становилось увеличение остаточной функциональной емкости легких и улучшение газообмена у некоторых больных. Традиционная ИВЛ с использованием соотношения вдох-выдох 1:2 или 1:1,2 подразумевает относительно долгую экспираторную фазу, значительно снижая среднее давление в дыхательных путях. При IRV соотношение фаз обычно составляет от 1,1:1 до 2:1, что может быть достигнуто относительно быстрым инспираторным потоком и его снижением для поддержания достигнутого давления в фазу вдоха. При применении IRV возникают два эффекта: а) удлинение времени вдоха ведет к увеличению среднего давления в дыхательных путях и открытию краевых альвеол, схожего результата достигают применением высокого ПДКВ; б) при более тяжелом поражении дыхательных путей, как результат перибронхиального сужения просвета терминальных отделов, с каждым вдохом происходит медленное выравнивание внутрилегочного давления, что приводит к неравномерной альвеолярной вентиляции. Эта неравномерность может стать причиной снижения перфузии альвеол с увеличением внутрилегочного шунтирования крови. При осторожном применении IRV, могут появляться воздушные ловушки, создающие внутреннее или аутоПДКВ, с селективным увеличинием интраальвеолярное давление в таких замкнутых полостях. Такой эффект может сочетаться с увеличением шунтирования и оксигенации. Внутреннее ПДКВ должно часто измеряться по причине возможного перерастяжения альвеол и вторичного респиратор-ассоциированного легочного повреждения. Несмотря на привлекательность возможности создания селективного ПДКВ при IRV, остается вопрос, добавляет ли данный эффект что-нибудь новое, помимо простого эффекта повышения среднего давления в дыхательных путях. Исследования, подобные проведенному Lessard, свидетельствуют о том, что вентиляция с контролем по давлению может быть использована для ограничения пикового инспираторного давления и нет значительных преимуществ PCV или PCIRV в сравнении с традиционной объемной ИВЛ с добавлением ПДКВ у пациентов с острой дыхательной недостаточностью. Данная точка зрения в дальнейшем была развита Shanholtz и Brower, которые задались вопросом применения IRV при лечении ОРДС. Вентиляция с освободждением давления (APRV)В основе APRV лежит режим постоянно положительного давления в дыхательных путях (СРАР). Короткий период более низкого давления позволяет выводить из легких СО2. Пациент имеет возможность дышать самостоятельно во время всего цикла аппаратного дыхания. Теоретическими преимуществами APRV являются более низкое давление в дыхательных путях и минутная вентиляция, мобилизация спавшихся альвеол, более высокий уровень комфорта пациента при спонтанном дыхании и минимальные гемодинами-ческие эффекты. Поскольку пациент сохраняет способность к самостоятельному дыханию благодаря открытому экспираторному клапану, данный режим легко переносится пациентами, отлучаемыми от седации или имеющими положительную динамику после черепно-мозговой травмы. Раннее начало применения данного режима приводит к улучшению гемодинамики и к мобилизации альвеол. К тому же существуют научные данные, доказывающие, что сохранение самостоятельного дыхания при данном режиме вентиляции снижает потребность в седации. Высокочастотная вентиляция легкихИнтерес к высокочастотной вентиляции легких (HFOV) у взрослых с острой дыхательной недостаточностью возник вследствие того, что традиционные режимы вентиляции могут индуцировать дальнейшее повреждение легких повторяющимся циклом открытия и закрытия дыхательных путей. При HFOV поддерживается относительно высокое среднее давление в дыхательных путях при установленном малом дыхательном объеме, который доставляется с высокой частотой. Таким образом, целью является достижение и поддержание легких открытыми при отсутствии большого давления прилагаемого к альвеолам. Большая часть опыта по применению данного метода описана в литературе по неонатальной и педиатрической практике. В только что опубликованном исследовании Mehta с соавт. 24 взрослых с ОРДС разной этиологии были вовлечены в проспективное исследование применения HFOV как «терапии спасения». Из этих пациентов 42% показали улучшение оксигенации и получили возможность вернуться к традиционным методам ИВЛ. Выжившие пациенты также провели меньшее количество дней на ИВЛ до перевода на HFOV, чем умершие. Требуются новые исследования, для того чтобы пролить свет на вопрос предполагаемой высокой эффективности данного режима у пациентов с ранними проявлениями ОРДС или ингаляционными поражениями. – Также рекомендуем “Адъювантная терапия при дыхательной недостаточности. Принципы” Оглавление темы “Интенсивная терапия в травматологии”:
|
Источник
