Перивентрикулярный отек что такое
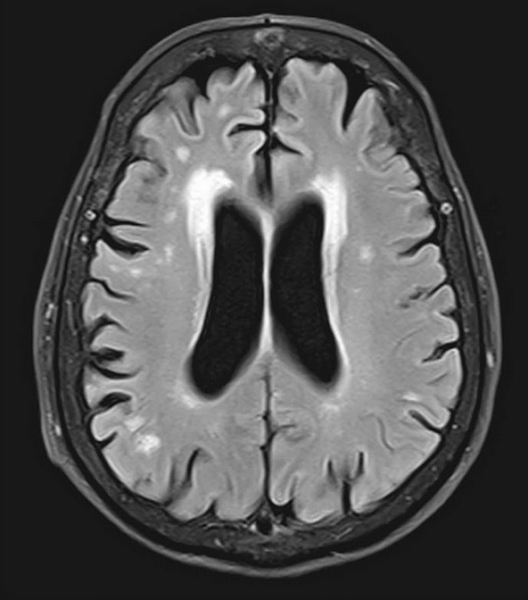
Почему возникает отек головного мозга, чем он грозит и как его предотвратить.
Мозг отвечает за все функции организма, поэтому, если он «выходит из строя», это влечет за собой множество проблем со здоровьем.
Что такое отек головного мозга?
Отек мозга – это ответная реакция организма на чрезмерные нагрузки или инфекцию. Обычно отек развивается очень быстро, однако так же быстро исчезает, если вовремя наложить лед или удалить избыточное количество жидкости. Если же отек мозга является результатом травмы или заболевания, вылечить его гораздо сложнее.
Для описания этого состояния также используется термин «повышенное внутричерепное давление», а также «церебральная эдема». Его суть заключается в том, что внутри черепной коробки повышается давление, в ответ на это нарушается мозговое кровообращение, а это, в свою очередь, приводит к отмиранию клеток мозга.
Причины отека головного мозга
Травма, болезнь, инфекция и даже перепад высот – любая из этих причин может привести к отеку мозга.
Черепно-мозговая травма (ЧМТ) – механическое повреждение внутричерепных структур. Возникает вследствие удара, падения, аварии. Зачастую ЧМТ осложняется ранением мозга отломками кости. Слишком сильный отек, в свою очередь, препятствует оттоку жидкости из ткани мозга.
Ишемический инсульт – наиболее распространенный тип нарушения мозгового кровообращения в результате образования тромба. В этом случае клетки мозга, не получая должного количества кислорода, начинают отмирать, и развивается отек.
Геморрагический инсульт – результат повреждения кровеносных сосудов мозга. Возникшее внутримозговое кровоизлияние приводит к повышению внутричерепного давления. Чаще всего геморрагический инсульт развивается из-за повышенного артериального давления, среди других причин – травма головы, прием некоторых лекарственных препаратов, а также врожденные пороки развития.
Инфекционные заболевания:
• Менингит – воспаление оболочки головного мозга, вызванное бактериями, вирусами и другими микроорганизмами, а также приемом некоторых медикаментов.
• Энцефалит – воспалительное заболевание мозга, вызванное группой вирусов, переносчиками которого обычно являются насекомые. Похожее состояние – энцефалопатия – наблюдается при синдроме Рейе.
• Токсоплазмоз – паразитарное заболевание, способное поразить ребенка еще в утробе матери. В группу риска входят также грудные дети и люди с ослабленной иммунной системой.
• Субдуральный абсцесс (Субдуральная эмпиема) представляет собой гнойную инфекцию (осложнение другого заболевания, например, менингита или синусовых инфекций), которая, быстро развиваясь, становится причиной отека мозга и препятствует оттоку жидкости из его тканей.
• Опухоль. Разрастаясь, она сдавливает участок мозга, нарушая кровообращение и вызывая отек окружающей ткани.
• Перепад высот. По неподтвержденным данным, высота более полутора километров над уровнем моря способна стать причиной отека мозга, что наблюдается при острой форме горной болезни (так называемый высокогорный отек мозга).
Симптомы отека мозга
Симптомы отека мозга варьируются в зависимости от причины и тяжести состояния. Как правило, признаки заболевания развиваются внезапно:
• Головная боль
• Боль или онемение в области шеи
• Тошнота, рвота
• Головокружение
• Неравномерное дыхание
• Нарушения зрения
• Амнезия
• Нарушение равновесия и походки (атаксия)
• Затруднение речи
• Понижение уровня сознания (ступор)
• Судороги
• Потеря сознания
Диагностика отека мозга
Выбор методов диагностики зависит от симптомов и предварительного диагноза. Общие обследования и тесты, используемые для диагностики отека мозга:
• Обследование шейно-головного отдела
• Неврологическое обследование
• КТ головного мозга – с целью определения величины и локализации отека
• МРТ головного мозга – с целью определения величины и локализации отека
• Анализ крови для определения возможных причин отека
Лечение отека мозга
Иногда симптомы отека головного мозга (например, вследствие легкой формы горной болезни или небольшого сотрясения) проходят самостоятельно через несколько дней. Однако в более серьезных случаях требуется незамедлительная медицинская помощь.
Лечение с помощью комбинации хирургических и медикаментозных методов направлено на снабжение мозга кислородом. В результате отек уходит. Как правило, своевременная терапия способствует более раннему и полному выздоровлению и заключается в следующем:
• Оксигенотерапия – искусственное введение кислорода в дыхательные пути (через ингалятор или другие приспособления). В этом случае насыщенная кислородом кровь лучше питает поврежденный мозг.
• Внутривенное вливание. Внутривенное введение лекарственных препаратов позволяет поддерживать давление и кровоток в норме, а также помогает бороться с возможной инфекцией.
• Понижение температуры тела (гипотермия) является эффективным методом коррекции отека мозга. Однако в настоящее время он используется еще недостаточно широко.
Лекарственные препараты. В некоторых случаях при отеке мозга назначаются медикаменты. Их выбор определяется в зависимости от причины и симптомов, сопровождающих развитие отека.
Вентрикулостомия представляет собой дренаж цереброспинальной жидкости из желудочков головного мозга через катетер. Данная операция выполняется для уменьшения повышенного внутричерепного давления.
Целью хирургического вмешательства при отеке мозга могут быть:
• Удаление фрагмента кости черепа, чтобы уменьшить внутричерепное давление. Эта операция называется декомпрессивной краниэктомией.
• Устранение причины отека, например, восстановление поврежденного кровеносного сосуда или удаление новообразования.
Осложнения отека головного мозга
Как правило, отек мозга имеет отдаленные последствия. Проблемы, с которыми вы можете столкнуться в будущем, зависят от тяжести и локализации повреждения. Возможно, это будут:
• Нарушения режима сна
• Рассеянность
• Нарушения двигательной активности
• Головные боли
• Депрессия
• Нарушения коммуникативных способностей
Конечно, врачи постараются свести к минимуму все эти негативные последствия.
Профилактика отека головного мозга
Чтобы избежать такой серьезной проблемы, как отек мозга, необходимо не забывать о правилах безопасности в повседневной жизни. Вот несколько простых правил:
• Всегда надевайте защитный шлем, когда вы ездите на велосипеде или на роликах, занимаетесь контактными видами спорта – выполняете какие-либо действия, при которых можно получить травму головы.
• Не забывайте о ремнях безопасности в автомобиле.
• Контролируйте и поддерживайте в норме артериальное давление.
• Не курите.
• Поднимаясь в горы, давайте себе время на акклиматизацию к высоте.
Источник
Перивентрикулярная лейкомаляция – это гипоксически-ишемическая энцефалопатия, характеризующаяся поражением белого вещества головного мозга новорожденных. Состояние чаще возникает у недоношенных, провоцируется патологиями течения беременности и родов, неадекватной респираторной поддержкой в постнатальном периоде. Заболевание проявляется мышечной дистонией, судорожным синдромом, задержкой психомоторного развития. Для диагностики болезни назначается КТ или МРТ мозга, ЭЭГ, допплерография церебральных сосудов. Лечение лейкомаляции включает медикаменты (нейропротекторы, инфузионные растворы, антиконвульсанты), индивидуальный комплекс физиотерапии, массажа, ЛФК.
Общие сведения
По разным данным, перивентрикулярная лейкомаляция (ПВЛ) встречается у 4,8-9% младенцев, причем среди больных преобладают недоношенные новорожденные (78%). Наибольшая вероятность появления болезни у детей, родившихся на сроке 27-32 недели. По данным аутопсии умерших младенцев, признаки ПВЛ регистрируются чаще – у 50-75%. Заболевание имеет большую значимость в детской неврологии, поскольку может вызывать тяжелые отдаленные последствия, считается ведущей причиной ДЦП.
Перивентрикулярная лейкомаляция
Причины
Основной этиологический фактор перивентрикулярной лейкомаляции – внутриутробная гипоксия, которая выступает следствием осложнений протекания беременности, материнских факторов риска либо негативного экзогенного воздействия. Также состояние может возникать при перинатальной гипоксии, которая развивается во время родов, в первые дни жизни младенца (при синдроме дыхательных расстройств, врожденных аномалиях сердца и легких, неонатальном сепсисе).
В группе риска наибольшую по численности категорию составляют недоношенные младенцы. Зачастую лейкомаляция выявляется у детей, которое были рождены от матерей с сахарным диабетом, хронической анемией, гипертиреозом либо страдавших от преэклампсии и эклампсии. Состояние возникает при выполнении экстренного кесарева сечения, неадекватном родовспоможении (травмирующие акушерские пособия). Высокая частота лейкомаляции (до 22%) отмечается при сочетании длительного безводного периода с хориоамнионитом у матери.
Патогенез
Поражение головного мозга связано со снижением кровотока в церебральных сосудах, недостаточным поступлением кислорода и питательных ингредиентов. Перивентрикулярная область наиболее чувствительна к этим изменениям, что обусловлено особенностями кровоснабжения, несовершенством процессов ауторегуляции, нейроонтогенетическими особенностями головного мозга у младенцев.
Недоношенные намного чаще страдают лейкомаляцией, поскольку у них на фоне гипоксии не увеличивается церебральный кровоток, как это бывает у рожденных в срок младенцев. В результате этого резко уменьшается кровоток в зоне между вентрикулофугальными и вентрикулопетальными артериями, быстро формируется гиперкапния и ацидоз. Расстройства микроциркуляции проявляются стазом, тромбозом, вне- и внутриклеточным отеком белого вещества.
При перивентрикулярной лейкомаляции в конечном итоге происходит некроз отельных участков мозгового вещества, образование кист, избыточное накопление медиаторов воспаления. Поскольку на 28-32 неделях в норме происходит активная миелинизация белого вещества, а в условиях гипоксии этот процесс не может происходить, недоношенные новорожденные впоследствии имеют серьезные органические поражения ЦНС.
Формирование ПВЛ возможно не только при недостатке кислорода, но и при гипероксии – при проведении ИВЛ, оказании других видов респираторной поддержки. При избыточном поступлении кислорода повышается рН крови в мозговой ткани, что вызывает рефлекторный спазм сосудов, затруднение венозного оттока. Также кислород активизирует процессы свободнорадикального церебрального повреждения.
Симптомы
Как правило, перивентрикулярная лейкомаляция формируется антенатально или на протяжении первых часов после рождения ребенка, поэтому начальные признаки заметны уже в родильном доме, особенно если младенец рожден недоношенным. При обширном повреждении белого вещества происходят нарушения сознания по типу летаргии или комы, однако возможна обратная симптоматика – повышенная возбудимость, оживление безусловных рефлексов, судорожный синдром.
Типичным проявлением патологии являются изменения тонуса мышц. На первом месяце жизни преобладает слабость мускулатуры ног в сочетании с нормальным формированием мышц верхних конечностей. У недоношенных новорожденных часто отмечается тотальная мышечная гипотония. Такие нарушения сохраняются в среднем до 6 месяцев, после чего они сменяются спастическими явлениями – повышением тонуса мускулатуры нижних конечностей, оживлением коленных рефлексов.
Течение перивентрикулярной лейкомаляции имеет неравномерный характер: периоды обострения симптоматики сменяются «мнимым благополучием», когда ребенок развивается относительно нормально. Затем происходит задержка формирования моторных навыков, развиваются различные сенсорные нарушения, дизартрия. 66% детей, особенно недоношенные, страдают от снижения остроты зрения вплоть до полной слепоты вследствие атрофии зрительных нервов.
Осложнения
Перивентрикулярные поражения белого вещества – крайне тяжелое состояние. Недоношенные дети с ПВЛ умирают в 50% случаев еще в период новорожденности, у выживших обычно наступает инвалидность с полной дезадаптацией. Пациенты с длительно сохраняющимся судорожными приступами в 85% случаев имеют грубую задержку психомоторного развития. У перенесших ПВЛ в будущем в 1,5 раза чаще встречаются фебрильные судороги, в 27 раз чаще формируется эпилепсия.
При множественных кистах в перивентрикулярной зоне у 80-97% больных (чаще – недоношенных) возникает детский церебральный паралич (ДЦП), который сопровождается глубоким психоречевым отставанием. Развитие заболевания связано с повреждением центральной части внутренней капсулы, средне- и заднелобных сегментов белого вещества полушарий. Также лейкомаляция вызывает микроцефалию (у 42% пациентов), нейросенсорную тугоухость (у 28% больных).
Диагностика
Постановка правильного диагноза в неонатальном периоде затруднена, что объясняется полиморфностью клинической картины, отсутствием патогномоничных симптомов. При физикальном осмотре выявляется асимметрия мышечного тонуса, патологическое усиление рефлексов, на более поздних этапах – спастическая диплегия. Особую настороженность следует проявлять в отношении детей, родившихся недоношенными. В план обследования новорожденных с подозрением на ПВЛ включаются:
- Нейровизуализация. При КТ и МРТ головного мозга определяются множественные очаги атрофии белого вещества, зачастую визуализируются кисты перивентрикулярной области размером более 4 мм, что коррелирует с тяжелым неврологическим дефицитом.
- Дуплексное сканирование сосудов. Исследование артерий головы и шеи с помощью допплерографии имеет важное значение для уточнения параметров кровотока, исключения сосудистых аномалий, которые могли быть причиной постнатальной гипоксии. По показаниям исследование дополняется реоэнцефалографией.
- ЭЭГ. При судорожном синдроме электроэнцефалография необходима для обнаружения зон мозга с повышенной электрической активностью. Недоношенным новорожденным требуются повторные исследования в разные возрастные периоды для оценки динамики морфофункционального созревания мозга.
- Консультации специалистов. При подозрении на патологию зрения, рекомендуется обследование у офтальмолога с осмотром глазного дна. Больным со сниженным слухом необходима консультация ЛОР-врача. Иногда требуется визит к детскому психологу, психиатру.
Лечение перивентрикулярной лейкомаляции
Терапия перивентрикулярной лейкомаляции представляет собой сложную задачу, учитывая необратимый характер повреждений белого вещества, частое сочетание гипоксически-ишемической энцефалопатии с поражениями других систем организма у недоношенных. Медикаментозное лечение подбирается на основе ведущих синдромов болезни и включает следующие группы препаратов:
- Инфузионная терапия. Растворы глюкозы, электролитов, витаминов оказывают положительное влияние на церебральный метаболизм, повышают устойчивость перивентрикулярных зон к гипоксии.
- Нейрометаболиты. Препараты улучшают кровоток и стимулируют доставку питательных веществ в головной мозг, а также выполняют функцию нейропротекторов, способствуют формированию когнитивных навыков.
- Антиконвульсанты. Для купирования судорог используются медикаменты из группы бензодиазепиновых транквилизаторов, а при их неэффективности применяются барбитураты, препараты для наркоза.
- Глюкокортикоиды. Лекарства показаны в случае осложнения заболевания внутричерепной гипертензией. В таком случае они дополняются осмотическими диуретиками.
Учитывая высокую частоту резидуальных неврологических явлений, рекомендовано восстановительное лечение. Чтобы улучшить двигательные способности, назначаются курсы массажа, физиотерапии, лечебной физкультуры. Для развития речевых навыков требуются коррекционные занятия у логопеда, дефектолога. Детям с поражением органов чувств нужна помощь тифлопедагога, сурдопедагога. Пациентам с ДЦП необходимы специальные ходунки, костыли, инвалидные коляски.
Прогноз и профилактика
В большинстве случаев лейкомаляция отличается неблагоприятным течением, отличается высоким уровнем смертности во время младенчества. Для выживших детей прогноз напрямую зависит от тяжести органического дефекта перивентрикулярной зоны, своевременности и полноты проведенного лечения. Профилактика ПВЛ включает рациональное ведение беременности, предупреждение родового травматизма, соблюдение протоколов при респираторной поддержке в роддоме, усиленный контроль за развитием недоношенных.
Источник

Патологические процессы, затрагивающие центральную нервную систему (ЦНС), влияют на работоспособность всего организма. Морфологические изменения зачастую носят необратимый характер, снижая функциональность поврежденных отделов.
Органические поражения головного мозга часто развиваются на фоне нарушения кровоснабжения интракраниального (внутричерепного) пространства. Следствием длительной ишемии нервных тканей может стать лейкоареоз – структурные изменения белого церебрального вещества.
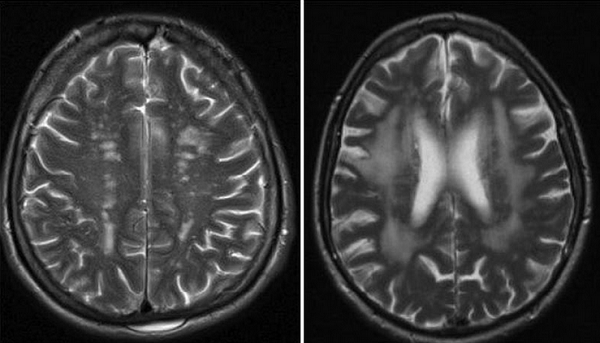
Признаки сосудистого поражения головного мозга
Своевременная диагностика заболевания позволяет стабилизировать работу брахиоцефальных артерий, снизить риск развития опасных осложнений. Эффективным методом исследования головного мозга является магнитно-резонансная томография.
МРТ предполагает использование силового поля, безвредного для здоровья человека. В ответ на направленный электромагнитный импульс наблюдается резонанс заряженных частиц в клетках организма. Атомы водорода в молекулах воды совершают колебательные движения, которые можно зарегистрировать при помощи чувствительных детекторов.
Информативность МР-сканирования зависит от насыщенности жидкостью изучаемых структур. Ткани головного и спинного мозга содержат большой объем воды, поэтому магнитно-резонансная томография позволяет визуализировать малейшие изменения в состоянии ЦНС.
Что такое лейкоареоз?
Причиной развития патологических процессов в области церебрального вещества служит хроническая ишемия головного мозга. При нарушении интракраниального кровообращения возникают очаги некроза нервной ткани. Структурные трансформации сопровождаются уменьшением плотности белого вещества, разрушением миелиновой оболочки нейронов. Процесс передачи нервных импульсов прекращается, снижается функциональность пораженного участка ЦНС.
В зависимости от локализации патологических явлений различают две формы лейкоареоза:
перивентрикулярный – дегенеративные процессы протекают в боковых желудочках головного мозга, возможны очаговые или диффузные изменения паренхимы;
субкортикальный – затрагивает белое вещество под корковым слоем.
Перивентрикулярный лейкоареоз как самостоятельное заболевание встречается редко, чаще данное явление служит симптомом другой патологии головного мозга. Причинами деструктивных процессов считают:
болезнь Альцгеймера;
рассеянный склероз;
болезнь Бинсвангера;
сосудистую деменцию;
ишемический инсульт;
гипертоническую болезнь;
сахарный диабет;
ВИЧ и пр.
Характерным признаком перечисленных патологий является нарушение мозгового кровообращения, приводящее к демиелинизации и дегенерации церебральных структур.
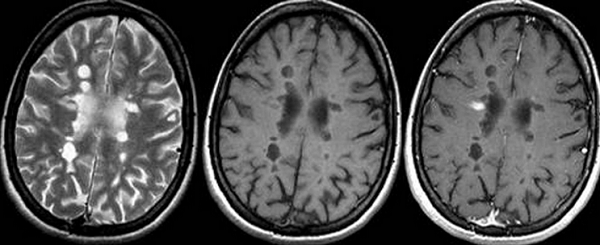
Перивентрикулярный процесс на снимках МРТ
К негативным факторам, повышающим риск развития лейкоареоза, относят:
пожилой возраст;
табакокурение;
алкоголизм;
употребление наркотических средств;
заболевания сердечно-сосудистой системы;
повышенную свертываемость крови;
нерациональное питание.
Перивентрикулярный процесс часто развивается вследствие отека головного мозга, сопровождающегося нарушением функционирования ликвора боковых желудочков. Крупные очаги появляются при лакунарном инфаркте или инсульте.
Симптомы лейкоареоза
Деструкция белого вещества характеризуется нарушением мозговых функций. Клинические проявления зависят от локализации и стадии патологического процесса. Степень поражения нервной ткани определяют с помощью инструментальных исследований. При проведении МРТ возможна диагностика лейкоареоза на начальном этапе.
Для клинической картины деструкции головного мозга характерны:
моторная дисфункция;
когнитивные нарушения;
расстройство психо-эмоционального фона;
нарушения речи;
мышечная слабость;
головные боли;
бессонница.
Первая стадия лейкоареоза сопровождается незначительными головокружениями, быстрой утомляемостью, слабостью. Пациент отмечает:
шум в ушах;
снижение концентрации внимания;
общее депрессивное состояние.
Возможны речевые нарушения, ослабление памяти. При осмотре выявляют повышение сухожильных рефлексов.
Вторая стадия протекает со значительным снижением функциональности организма. Отмечают:
нарушение координации движений;
потерю равновесия при ходьбе;
замедление психомоторных функций;
частичную или полную утрату речи;
снижение памяти и внимания.
Пациент перестает контролировать свои действия. Заметны апатия, раздражительность, депрессия. Возможны учащенное мочеиспускание, ночной диурез.
Третья стадия сопровождается усилением перечисленных признаков. Наблюдаются:
выраженные поведенческие нарушения;
падения при ходьбе;
утрата речи, памяти;
недержание мочи.
Пациент не способен к самообслуживанию.
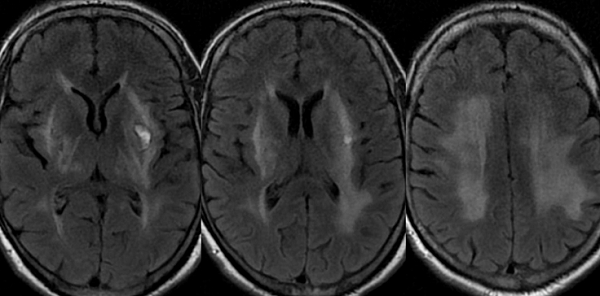
Лейкоареоз на снимках МРТ
Деструкция белого вещества в области лобной доли характеризуется снижением интеллектуальных способностей на фоне удовлетворительной моторной функции.
МРТ головного мозга покажет лейкоареоз?
Магнитно-резонансную томографию считают одним из наиболее информативных способов исследования церебральных структур. В результате МРТ получают послойные изображения с шагом от 1 мм.
Сканирование проводят в трех взаимно перпендикулярных проекциях, при необходимости врач реконструирует 3D-модель рассматриваемой области. Томограммы визуализируют строение, форму, размеры интракраниальных структур. Трехмерная проекция помогает оценить локализацию и распространенность патологического процесса.
Изменения, характерные для лейкоареоза, хорошо видны при МРТ головного мозга. Метод позволяет оценить состояние белого вещества, показывает нарушение целостности миелинового слоя нейронов. Для визуализации кровеносной системы назначают МР-ангиографию.
Исследование церебральных сосудов проводят с использованием контрастного препарата. После внутривенной инъекции раствор заполняет кровеносное русло и межклеточное пространство. Томограммы дают возможность оценить просвет, наполненность, состояние стенок сосудов. В результате ангиографии выявляют патологии церебральных вен и артерий, последствия нарушений мозгового кровообращения (ишемию и пр.)
Сканирование применяют для дифференциальной диагностики дегенеративно-дистрофических, воспалительных, демиелинизирующих процессов, следствием которых может стать деструкция белого вещества. МРТ показывает структурные изменения тканей головного мозга, помогая выявлять пораженные очаги диаметром от 3 мм.
Магнитно-резонансная томография позволяет определить лейкоареоз на начальном этапе, уточнить патогенез заболевания и выбрать результативный метод лечения. Эффективность терапевтических и хирургических мер во многом зависит от этиологии деструктивного процесса.
Признаки легкого перивентрикулярного лейкоареоза на МРТ
Заболевание развивается на фоне увеличения количества жидкости вокруг боковых желудочков головного мозга. Расширение периваскулярной щели сопровождается образованием патологических очагов вследствие инсульта или инфаркта. Наблюдается нарушение кровотока церебральных артерий.
При проведении МРТ выявляют следующие признаки лейкоареоза:
вдоль перивентрикулярного пространства заметна равномерная полоса;
над полюсом бокового желудочка образуется «шапочка», соответствующая пораженному участку белого вещества.
На Т2-взвешенных изображениях патологические очаги имеют гиперинтенсивный сигнал.

Изменения в области боковых желудочков при перивентрикулярном лейкоарезе
Клиника «Магнит» в Санкт-Петербурге проводит МРТ головного мозга на закрытом томографе фирмы Siemens. Устройство генерирует силовое поле напряженностью 1,5 Тл, обеспечивая высокое качество снимков. Записаться на исследование можно по телефону +7 (812) 407-32-31 или на сайте клиники.
Источник
