Периневральный отек что это такое
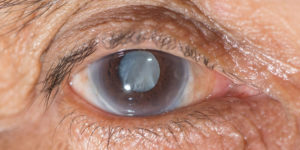
Периферические отеки
Периферические отеки могут возникать по разным причинам, начиная от побочного действия лекарств, заканчивая сердечной или почечной патологией. Симптом не возникает сам по себе, а часто указывает на серьезное заболевание.
Отечность определяется визуально и пальпаторно – после надавливание остается ямка (как видно на фото).
 Наиболее часто периферические отеки развиваются в области голеней и стоп
Наиболее часто периферические отеки развиваются в области голеней и стоп
Периферические отеки – что это такое?
Отек периферических тканей возникает из-за накопления воды в подкожной клетчатке. Это не отдельная патология, а следствие какого-либо заболевания.
В основном отечность локализуется на ногах, в области голеней и стоп. Реже наблюдается другая локализация:
- лицо;
- шея;
- поясница;
- верхние конечности.
Механизм развития может быть разным, в связи с чем выделяют несколько разновидностей отеков:
- Гидростатические. Задержка жидкости возникает вследствие повышения гидростатического давления.
- Гипопротеинемические. Развиваются из-за низкого уровня белков в крови.
- Воспалительные. Их причиной является повышение проницаемости стенки капилляров.
Возможные причины
Существует несколько причин, по которым развиваются периферические отеки. Все они разделяются на системные и местные.
К наиболее частым системным причинам относится патология сердца, почек, печени, щитовидной железы, к местным – тромбоз глубоких вен, хроническая венозная недостаточность.
Читайте также:
8 симптомов почечной недостаточности
Тромбоз глубоких вен: 8 симптомов, сигнализирующих об опасности
5 симптомов, при которых необходимо обратиться к эндокринологу
Симптомы
На что важно обращать внимание при возникновении отечности:
- Скорость развития. Если симптомы развились резко, в течение трех суток – скорее всего причина заключается в тромбозе глубоких вен. При остальных патологиях симптомы прогрессируют медленнее.
- Локализация. Поражение только одной конечности указывает на местную причину (например, тромбоз или лимфатический отек). При сердечной недостаточности чаще возникает отечность ног, при почечной – лица.
- Болезненность. Чаще всего отечная зона безболезненна, но при тромбозе присутствует выраженная боль в пораженной конечности.
- Время суток, когда симптом выражен сильнее. Если отечность проходит после ночного отдыха, это указывает на венозную недостаточность.
- Состояние кожных покровов. При лимфатическом отеке кожа над зоной поражения уплотнена, при венозной недостаточности – коричневого цвета. В остальных случаях кожа не меняется.
Жидкость может накапливаться не только в периферических тканях, но и в полостях организма:
- в брюшной полости (асцит);
- в грудной полости (гидроторакс);
- в полости перикарда (гидроперикард).
Часто наблюдаются и другие симптомы, указывающие на первичное заболевание. Например, боль в сердце и одышка при сердечной недостаточности, уменьшение выделения мочи при поражении почек и т. д.
Диагностика
Периферические отеки – это повод обратиться за медицинской помощью. Врач проведет тщательное обследование: пальпацию отеков, аускультацию сердца и легких, перкуссию печени.
При необходимости назначаются дополнительные анализы, которые помогут выявить причину патологического процесса.
Как лечить патологию
Основное направление лечения – устранение причины.
Конкретные медикаментозные препараты назначает врач, самолечение в этом случае может только навредить.
Вне зависимости от причины необходимо откорректировать питание:
- Уменьшить потребление соли.
- Ограничить потребление молочного и соленого, особенно перед сном.
- Основу рациона должны составлять овощи, фрукты и белки.
Симптоматическое лечение заключается в назначении диуретиков – препаратов, которые стимулируют выведение жидкости. Назначается Фуросемид, Торасемид, Гипотиазид, Спиронолактон.
Профилактика заключается в прохождении медицинских осмотров, своевременном лечении заболеваний, соблюдении диеты.
Видео
Предлагаем к просмотру видеоролик по теме статьи.
Нашли ошибку в тексте? Выделите ее и нажмите Ctrl + Enter.
Источник
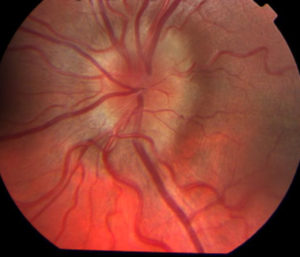 Отек зрительного нерва (ЗН) — это результат повышения давления внутри черепа, которое происходит за счет различных патологических процессов, протекающих в организме. Спектр варьируется от врожденных пороков развития, опухолей, лекарств, травм, воспалений до других заболеваний глаз, таких как глаукома, которые могут привести к вторичному повреждению ЗН и его отечности.
Отек зрительного нерва (ЗН) — это результат повышения давления внутри черепа, которое происходит за счет различных патологических процессов, протекающих в организме. Спектр варьируется от врожденных пороков развития, опухолей, лекарств, травм, воспалений до других заболеваний глаз, таких как глаукома, которые могут привести к вторичному повреждению ЗН и его отечности.
Анатомия зрительного нерва
ЗН — это вторая пара черепно-мозговых нервов, которым свойственные зрительные раздражения. Состоит из 4 отделов — внутричерепного, внутриканальцевого, внутриглазного и внутриорбитального.
ДЗН — это диск ЗН, он представляет собой место соединения оптических волокон. Его длина — 1 мм, диаметр — 1,75–2 мм. Находится ДЗН в носовой части глазного дна.
Вторая пара черепных нервов окружена тремя мозговыми оболочками. Его толщина — 3–3,5 мм, длина — 3,5–5,5 см. Волокна ЗН различны по направлению и калибру, есть тонкие и толстые. Последние передают световое раздражение в зрительную часть коры, первые — это рефлекторные, они необходимы для передачи светового импульса в парасимпатическую нервную систему.
Причины отека зрительного нерва
Неврит
Причина и происхождение в значительной степени неизвестны, но врачи рассматривают рассеянный склероз. Пострадавшие пациенты страдают от ослабления зрения, насыщения цвета (особенно красного) и болезненного движения глазами.
Симптомы переходные, то есть они, как правило, формируются самостоятельно. Если поражена задняя часть ЗН (ретробульбарный неврит), то воспаление и отек диска зрительного нерва могут быть не диагностированы при осмотре глазного дна. Необходимы другие методы визуализации.
Оптическая нейропатия
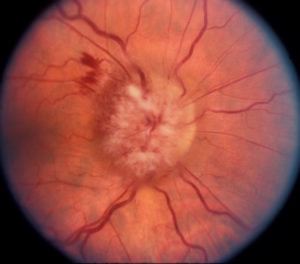 В случае острого закрытия кровеносных сосудов глаза ЗН необратимо повреждается, без подачи кислорода и питательных веществ через кровь нейроны ЗН отмирают. Поскольку эти клетки не могут вновь образоваться, постепенно снижается зрение до слепоты. Офтальмолог при осмотре видит бледный отекший зрительный нерв-сосочек и его головку, небольшие кровотечения. Пациент замечает сильное ухудшение зрения и ограничение поля зрения.
В случае острого закрытия кровеносных сосудов глаза ЗН необратимо повреждается, без подачи кислорода и питательных веществ через кровь нейроны ЗН отмирают. Поскольку эти клетки не могут вновь образоваться, постепенно снижается зрение до слепоты. Офтальмолог при осмотре видит бледный отекший зрительный нерв-сосочек и его головку, небольшие кровотечения. Пациент замечает сильное ухудшение зрения и ограничение поля зрения.
Атеросклероз или эмболия из-за болезни сердца (фибрилляция предсердий/эндокардит) являются наиболее распространенными причинами. Артериит височной артерии, аутоиммунный цистит, вызывают оптическую нейропатию.
Патологии внутренних органов
К развитию патологии приводят некоторые болезни внутренних органов. Например, инсульт, гипертония и почечная недостаточность.
Для каждого состояния характерны определенные признаки, их легко различить при проведении соответствующей диагностики.
Артерии височной артерии
Это аутоиммунное заболевание, приводящее к сосудистому воспалению (васкулит). Примерно в 30% случаев поражены глазные артерии, это приводит к ослаблению зрения вплоть до слепоты.
Пациент часто страдает от сильной головной боли, испытывает трудности с пережевыванием пищи. При физическом обследовании височная артерия болезненна. Если поражены глаза, то специалист видит признаки отекшего зрительного диска.
Глаукома
 Глаукома является следствием патологически повышенного давления в глазах. Она повреждает зрительный нерв, точнее сосок. Пациент замечает ухудшение зрения и выпадение поля зрения.
Глаукома является следствием патологически повышенного давления в глазах. Она повреждает зрительный нерв, точнее сосок. Пациент замечает ухудшение зрения и выпадение поля зрения.
Атрофия зрительного нерва
Атрофия зрительного нерва обозначает необратимое повреждение ткани ЗН. Первичная форма, обусловленная врожденной неисправностью, отличается от вторичной. В последнем случае, причиной являются другие заболевания или механические факторы. Возможные факторы:
- сильное давление на ЗН;
- нарушение кровообращения;
- воспаление;
- интоксикация.
Данные состояния характеризуются отеком зрительной головки, дефектами поля зрительного восприятия и ухудшением остроты.
Другие причины
Отек ЗН развивается из-за повышения давления внутри черепа, связанного с гнойными абсцессами в пространстве черепа, внутренними кровотечениями, ЧМТ. Причиной отека ДЗН выступает краниосиностоз и менингит, энцефалит.
Группа риска
Предрасположенность к данному состоянию имеется у всех пациентов с глазными заболеваниями, травмами головного мозга. Больше всего отеку подвержены личности со слабой иммунной системой и опухолями.
Классификация
Отек зрительного нерва бывает двусторонним или односторонним. В первом случае поражается оба органа оптической системы, во втором — лишь один.
При одностороннем отеке ЗН симптоматика слабо выражена, даже опытные офтальмологи не всегда замечают отечность.
Заболевание имеет острый и хронический характер. При остром течении развитие клинической картины спонтанное, симптоматика появляется в течение 2–3 часов.
При повторяющихся рецидивах на развитие первых признаков уходит до 3 дней.
Симптомы
Клиническая картина характеризуется постепенным снижением остроты зрительного восприятия. Особенно сильно ухудшается в центральной части поля зрения.
Периодически затуманивается зрение, нарушается цветовосприятие, умеренно напрягаются вены и отсутствуют очаги.
Поражение нервных волокон приводит к двоению в глазах, головным болям, мерцаниям перед глазами, тошноте и рвоте.
Дальнейшее прогрессирование патологического состояния приводит к образованию скотом в поле зрения. Возможно развитие вторичной атрофии ЗН.
Диагностика
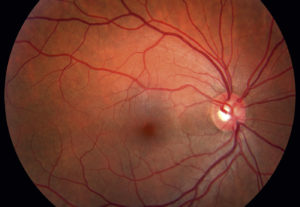 Первичное обследование проводится с помощью офтальмоскопа. Это визуальная оценка состояния головки ЗН, артерий и вен сетчатки. Обязательно проводят реакцию зрачка на свет с помощью небольшой лампы. Как правило, оба зрачка одинаково сильно сужаются, независимо от того, на какой орган зрения врач направит световой конус.
Первичное обследование проводится с помощью офтальмоскопа. Это визуальная оценка состояния головки ЗН, артерий и вен сетчатки. Обязательно проводят реакцию зрачка на свет с помощью небольшой лампы. Как правило, оба зрачка одинаково сильно сужаются, независимо от того, на какой орган зрения врач направит световой конус.
Однако при ретробульбарном неврите часто наблюдается так называемый относительный афферентный дефект зрачка.
Это означает, что ЗН пораженного глаза не так хорошо направляет входящие световые сигналы в мозг, как другой ЗН. В результате зрачки сужаются меньше, когда врач наводит свет на больной глаз. Для более детального осмотра нервных волокон используют специальные капли, расширяющие зрачки.
При необходимости проводят дополнительные исследования. С их помощью выясняют, какая причина привела к отеку ЗН. Для диагностики рассеянного склероза проводят МРТ головы и позвоночника.
Проводится поясничная пункция для забора спинномозговой жидкости. Она проверяется на наличие признаков воспалительного процесса.
Лечение
Если имеется ретробульбарный неврит, используются препараты, подавляющие иммунную систему (иммунодепрессанты). Вводятся глюкокортикоиды (стероиды), такие как Кортизон или Метилпреднизолон. Первые пять дней препараты используют в высоких дозах, затем медленно снижают дозировку в течение следующих 2 недель.
 Перед тем, как проводить терапию с помощью Кортизона, необходимо исключить такие заболевания, как туберкулез, язва желудка, сахарный диабет или гипертония. Они могут ухудшаться при глюкокортикоидном лечении. Если бактериальная инфекция является причиной отека зрительного нерва, для лечения могут быть использованы антибиотики.
Перед тем, как проводить терапию с помощью Кортизона, необходимо исключить такие заболевания, как туберкулез, язва желудка, сахарный диабет или гипертония. Они могут ухудшаться при глюкокортикоидном лечении. Если бактериальная инфекция является причиной отека зрительного нерва, для лечения могут быть использованы антибиотики.
Стероиды тоже могут оказаться полезными для остановки данной иммунной реакции.
Терапия дополняется мочегонными средствами. Они нормализуют баланс спинномозговой жидкости. В тяжелых случаях показано оперативное вмешательство.
Осложнения
Основным осложнением отека зрительного нерва является постепенное ухудшение зрения и полная слепота, наступающая при отсутствии лечения.
Прогноз
Что касается течения и прогноза отека зрительного нерва, то необходимо опираться на причину заболевания и тяжесть ее течения. Как правило, в первые три недели еженедельно следует посещать офтальмолога.
Прогноз всегда благоприятный, если терапия начата своевременно.
Профилактика
Предотвратить развитие болезни можно. Профилактика предполагает своевременное обращение в больницу при получении травм, появлении признаков глазных заболеваний.
В данный перечень входит соблюдение правил личной гигиены. Во избежание развития инфекций, которые в дальнейшем способны вызвать отек ЗН, нельзя тереть глаза грязными руками и пользоваться чужими косметическими средствами/полотенцами.
Полезное видео
Была ли статья полезной?
Оцените материал по пятибалльной шкале!
Если у вас остались вопросы или вы хотите поделиться своим мнением, опытом – напишите комментарий ниже.
Что еще почитать
Источник
Недостаток ингибитора С1-эстеразы (С1-INH) – редкая патология иммунной системы, вызывающая спонтанные приступы ангионевротического отека из-за избытка брадикинина. Они доставляют пациенту большой дискомфорт, приводят к психоэмоциональным расстройствам, ухудшают качество жизни и могут быть опасными для жизни. Ангионевротический отек, вызванный брадикинином, – редкое заболевание, обычно наследуемое по аутосомно-доминантному типу.
Ангионевротический отек – распространенный симптом в клинической практике, с которым может столкнуться любой врач. Следовательно, очень важно уметь распознавать и дифференцировать происхождение этого клинического симптома.
Что такое ангионевротический отек
Ангионевротический отек – это внезапный отек более глубоких слоев кожи и подкожной клетчатки. Этот симптом при крапивнице может сочетаться с высыпанием волдырей. В этом случае ангионевротический отек вызван высвобождением гистамина. Отек Квинке также может развиваться при количественной или качественной дисфункции компонентов комплемента. В этом случае ангионевротический отек диагностируется как отдельное заболевание.
![]() Крапивница
Крапивница
Белок, регулирующий комплемент, C1-INH – это фермент, который регулирует количество брадикинина в организме. Недостаток этого фермента вызывает ангионевротический отек, поскольку он нарушает регуляцию систем калихреина и хинина и приводит к выработке значительно большего количества брадикинина.
Дефицит C1-INH может быть как врожденным, так и приобретенным. Наследственный ангионевротический отек, вызванный дефицитом C1-INH, встречается у 1 из 50000 человек. У людей приобретенный ангионевротический отек, вызванный дефицитом C1-INH, встречается еще реже – 1 на 600 тыс. людей в мире.
Цель статьи – обзор патогенеза, диагностики, дифференциальной диагностики и принципов лечения ангионевротического отека с дефицитом C1-INH.
Клиническое проявление и дифференциальный диагноз
В научной литературе ангионевротический отек может быть обозначен как отек Квинке, ангионевротический отек, гигантская крапивница. При ангионевротическом отеке изменения происходят в глубоких слоях кожи и под кожей. Клинически это проявляется в виде асимметричного отека и припухлости определенного участка тела.
Одним из распространенных сопутствующих и раздражающих пациентов симптомов является боль. Кожа в месте инъекции может оставаться неизменной или может возникнуть покраснение размытых линий. Отек сохраняется до 72 часов или даже дольше.
Ангионевротический отек может возникнуть на любом участке тела – губах, языке, лице, конечностях и т.д. При каждом приступе ангионевротического отека опухоль и припухлость могут быть на разных участках.
- Ангионевротический отек лица вызывает дискомфорт и нарушает повседневную деятельность.
- Ангионевротический отек гортани – острое и опасное для жизни состояние. При отсутствии лечения ангионевротический отек гортани приводит к смерти примерно в 25-40% случаев. У любого пациента с дефицитом C1-INH приступ ангионевротического отека гортани может возникнуть хотя бы один раз в жизни.
- Отек Квинке также может возникать во внутренних органах, таких как стенка кишечника. Это вызывает боли в животе, тошноту, рвоту, диарею, общую слабость – все эти симптомы относят к острому абдоминальному синдрому, наиболее частой причиной которого является аппендицит.
![]() Отек Квинке
Отек Квинке
Своевременное распознавание ангионевротического отека из-за дефицита C1-INH может обеспечить соответствующее лечение и избежать ненужного хирургического вмешательства. Это важно, так как клинические исследования показали, что пациенты с дефицитом C1-INH часто подвергались ненужным хирургическим вмешательствам. При соответствующем лечении можно предотвратить или снизить частоту спонтанного ангионевротического отека.
Ангионевротический отек диагностируется на основании истории болезни пациента и объективного обследования. Патологию следует дифференцировать от:
- Анасарка – это широко распространенный отек мягких тканей, которое является симметричным и является клиническим признаком других заболеваний, таких как недостаточность почек, микседема;
- Псевдоангионевротического отека, например, при синдроме компрессии верхней полой вены;
- Синдрома Мелкерссона-Розенталя – нейропатии, которая клинически может проявляться отеком лица или губ).
Ангионевротический отек из-за дефицита C1-INH встречается гораздо реже и устойчив к лечению антигистаминными препаратами, системными глюкокортикоидами и адреналином.
Если подозревается ангионевротический отек из-за дефицита C1-INH, рекомендуется тест на компонент комплемента 4 (C4). C4 снижается даже при ремиссии и всего на 5% у всех пациентов остается неизменным или повышенным.
Диагноз подтверждается исследованием активности (функции) и количества C1-INH. Также проводится тестирование на антитела к C1-INH. При наследственном ангионевротическом отеке титр антител C1-INH в норме, а при приобретенном ангионевротическом отеке снижается у 70% пациентов.
Роль C1-INH и патогенез ангионевротического отека из-за дефицита
C1-INH C1-INH непосредственно участвует в системе калькреина и кинина, а также в регуляции медиатора воспаления брадикинина. Недостаток этого фермента приводит к нарушению метаболических путей калихреина и кинина и чрезмерной продукции брадикинина.
Ангионевротический отек из-за дефицита C1-INH делится на четыре типа, основные отличия которых представлены в таблице 1. C1-INH является представителем семейства серпинов, ингибитором сериновой протеазы. Ген C1-INH находится на хромосоме 11 и называется SERPING1. Именно мутации в этом гене вызывают дефицит C1-INH.
Если мутация в этом гене обнаружена, ангионевротический отек классифицируется как первый тип, т.е. ангионевротический отек, наследуемый по аутосомно-доминантному типу. Около 75%. пациентов с этой мутацией указывают на то, что случаи этого заболевания находятся в семье, но около 25%. Мутация de novo выявляется во всех случаях заболевания.
При третьем типе ангионевротического отека эндогенный C1-INH ингибирует протеазы и факторы (например, XII и XIIa), участвующие в физиологических каскадах систем комплемента, калькреина и кинина. Эти системы участвуют в таких процессах, как коагуляция и фибринолиз.
Фактор XII автоматически активируется с образованием фактора XIIa, который расщепляет прекаликреин, который, в свою очередь, генерирует плазменный калькреин. Каликреин в плазме активирует фактор XII, который регенерирует фактор XIIa и расщепляет макромолекулярный кининоген, высвобождающий брадикинин.
Медиатор воспаления брадикинин связывается с рецепторами В2, которые находятся на поверхности клетки, и образуют комплекс. Этот комплекс вызывает расширение сосудов, увеличивает проницаемость эндотелия сосудов. Весь каскад этих процессов вызывает ангионевротический отек.
Снижение уровня C1-INH выявляется не во всех случаях. Количество этого фермента может быть достаточным, но функция может быть нарушена. Такой патогенез характерен как для врожденного, так и для приобретенного ангионевротического отека.
Таблица 1. Типы ангионевротического отека из-за дефицита C1-INH
| Первый тип | Второй тип | Третий тип | Четвертый тип |
| Врожденный | Врожденный | Врожденный | Приобретенный |
| C1-INH – это C4 ↓, C1q – норма | Уровни C1-INH и C4, C1q являются нормой | Уровни C1-INH и C4, C1q являются нормой | Количество C1-INH и C4, C1q ↓ |
| Функция C1-INH не нарушена | Функция C1-INH нарушена или нормальна | Функция C1-INH не нарушена | Функция C1-INH нарушена |
| Мужчины и женщины – 1: 1 | Мужчины и женщины – 1: 1 | Мужчины < женщины | Мужчины и женщины – 1: 1 |
| 85 процентов. во всех случаях дефицита C1-INH | 15 процентов во всех случаях дефицита C1-INH | Наименее распространенный тип | Очень редко |
| Пациенты младше 20 лет | Пациенты младше 20 лет | Больные женщины старше 40 лет | Больные люди более 40 лет пациентов |
| Мутация на хромосоме 11 (SERPING1) *. Унаследовано по аутосомно-доминантному типу. 75%. семейный анамнез (+) , 25% – мутация de novo | Точечная мутация | Мутации в генах ANGPT1 * или PLG * | Может спровоцировать сопутствующие заболевания гематологического или аутоиммунного происхождения. Нет семейной истории |
* SERPING1 – англ. Ингибитор серпин-пептидазы Clade G Member 1, ANGPT1 – ангиопротеин 1, PLG – плазминоген.
Принципы лечения отека Квинке, вызванного дефицитом C1-INH
Чтобы избежать приступов отека Квинке, рекомендуется избегать провокационного фактора, который может включать стресс, травму или оральные контрацептивы. Однако часто основная причина отека Квинке неизвестна, и он возникает спонтанно.
Ангионевротический отек из-за дефицита C1-INH не связан с крапивницей или другими аллергическими заболеваниями, при которых гистамин является одним из основных факторов патогенеза. Следовательно, лечение ангионевротического отека, вызванного брадикинином, антигистаминными препаратами, глюкокортикоидами и / или адреналином неэффективно.
Для лечения ангионевротического отека из-за дефицита C1-INH может быть назначено симптоматическое или профилактическое лечение. Симптоматическое лечение – это прием лекарства во время приступа ангионевротического отека.
![]() Симптоматическое лечение ангионевротического отека
Симптоматическое лечение ангионевротического отека
Основные препараты, применяемые при приступах приобретенного и врожденного острого ангионевротического отека, – концентрат C1-IHN, антагонист рецептора B2 икатибант и ингибитор каликреина экалантид. Если эти препараты недоступны, возможно лечение плазмой, обработанной растворителем-детергентом (SDP) или свежезамороженной плазмой.
Профилактическое лечение – это прием медикаментов для предотвращения приступа отека Квинке. Оно может быть краткосрочным или долгосрочным.
- Цель длительного профилактического лечения – снизить частоту и тяжесть спонтанных приступов ангионевротического отека. Длительное профилактическое лечение считается эффективным, когда частота возникновения ангионевротического отека снижается более чем на 50%.
- Цель краткосрочного профилактического лечения – предотвратить ангионевротический отек во время запланированной процедуры или вмешательства, например, вмешательства стоматологического происхождения.
Лекарства для лечения отека Квинке, вызванного дефицитом C1-INH
Для симптоматического и профилактического лечения используется производное C1-INH в плазме крови, которое увеличивает концентрацию C1-INH в плазме. Синтетический концентрат C1-INH человека используется для лечения ангионевротического отека с 1970-х годов. В настоящее время также вводятся синтетические концентраты C1-INH. Исследования показали, что использование производного плазмы C1-INH в дозе 1000 МЕ 2 м.т. в неделю снижает частоту спонтанных приступов ангионевротического отека на 50% по сравнению с плацебо.
Синтетические андрогены – даназол и станозол – используются как в краткосрочной, так и в долгосрочной профилактике. Результаты двойного слепого плацебо-контролируемого исследования показали, что андрогены снижают тяжесть и частоту ангионевротического отека. Правда, такое лечение связано с риском побочных эффектов. Наиболее частые побочные эффекты, вызываемые андрогенами, – увеличение волос, вес, артериальное давление, активность ферментов печени и изменение голоса.
![]() Синтетический андроген – даназол
Синтетический андроген – даназол
Angioedem также лечится экалантидом. Это рекомбинантный белок из 60 аминокислот, прямой ингибитор каликреина. Исследования показали, что он сокращает продолжительность отека Квинке примерно на 5%. У всех испытуемых наблюдались аллергические реакции. Эккалантид лучше всего подходит для лечения острого ангионевротического отека.
Еще одно лекарство, используемое для лечения ангионевротического отека, – это икатибант, антагонист рецептора B2. Хорошо переносится. По данным недавних клинических испытаний, икатибант составляет примерно 80%. Нежелательные явления наблюдались не у всех пациентов. Икатибант показал свою эффективность при лечении ангионевротического отека 1 и 2 типа и ангионевротического отека, вызванного АПФ.
Последнее эффективное лечение – это биологическая терапия ланаделумабом. Это моноклональные антитела, которые связываются с активным калькреином в плазме. В клинических испытаниях ланаделумаб был эффективен для длительного профилактического лечения и вызывал несколько побочных эффектов. При лечении наследственного ангионевротического отека этот препарат оказался более эффективным, чем плацебо.
Лечение ангионевротического отека, вызванного дефицитом C1-INH, кратко изложено в таблице 2.
Таблица 2. Лечение отека Квинке, вызванного дефицитом C1-INH
| Острое состояние – во время приступа отека Квинке | Краткосрочная профилактика | Долгосрочная профилактика |
| Избегайте провокационных факторов: стресса, напряжения, пероральных контрацептивов и т.д. | ||
| Внутривенное вливание производного плазмы C1-INH (человеческого или рекомбинантного) | Цель – предотвратить ангионевротический отек во время запланированной процедуры или вмешательства | Цель – снизить частоту и тяжесть приступов спонтанного ангионевротического отека |
| Икатибант подкожная инъекция (антагонист рецептора брадикинина B2) | Инфузия производного плазмы C1-INH | Инфузия производного плазмы C1-INH |
| Подкожная инъекция эскалантида (ингибитор плазменного каликреина, предотвращающий превращение кининогена в брадикинин) | Препараты тестостерона: данозол, станозол | Препараты тестостерона: данозол, станозол |
| Интубация, трахеостомия | Икатибант | Икатибант |
Резюме
Ангионевротический отек из-за дефицита C1-INH – редкая патология. Он может быть как врожденным, так и приобретенным. Ангионевротический отек может возникнуть в любом месте тела. Отек гортани – распространенное и опасное для жизни состояние.
Ангионевротический отек из-за дефицита C1-INH диагностируется при выявлении дефицита или дисфункции компонента этой системы комплемента. Препарат выбора для лечения – концентрат C1-INH. Его можно использовать во время острого приступа отека Квинке или для долгосрочной и краткосрочной профилактики.
Источники: Ридл М.А., Гривчева-Пановская В., Молдован Д. и др. Рекомбинантный ингибитор С1-эстеразы человека для профилактики наследственного ангионевротического отека: многоцентровое рандомизированное двойное слепое плацебо-контролируемое перекрестное исследование фазы 2. Ланцет, 2017; Буссе П.Дж., Смит Т. Гистаминергический ангионевротический отек. Клиники иммунологии и аллергии Северной Америки, 2017; Ловерде Д., Files DC, Кришнасвами Г. Ангионевротический отек. Реанимационная медицина, 2017; Radonjic-Hoesli S, Hofmeier KS, Micaletto S, et al. Крапивница и ангионевротический отек: обновленная информация о классификации и патогенезе. Клинические обзоры в аллергии и иммунологии, 2017; Зеерледер С., Леви М. Наследственный и приобретенный C1-ингибитор-зависимый ангионевротический отек: от патофизиологии к лечению. 2016; Заничелли А., Азин Г.М., Ву М.А. и др. Диагностика, течение и лечение отека Квинке у пациентов с приобретенным дефицитом ингибитора C1. Журнал аллергии и клинической иммунологии: на практике, 2017; Буссе П.Дж. и др. Ланаделумаб для профилактического лечения наследственного ангионевротического отека с дефицитом ингибитора С1: обзор доклинических исследований и исследований фазы I. BioDrugs, 2018; Хориучи Т. Наследственный ангионевротический отек с 1888 по 2018 год – прогресс и проблемы. Демпстер Дж. (2018). Практические аспекты применения концентрата C1-INH в уменьшенном объеме для лечения наследственного ангионевротического отека: практический опыт. Аллергия, астма и клиническая иммунология, 2018; Фирст Р., Даффи Х. (2015). Лечение острых приступов наследственного ангионевротического отека: роль экалантида. Journal of Blood Medicine, 2015; Banerji A, et al. Эффект ланаделумаба по сравнению с плацебо на профилактику наследственных приступов ангионевротического отека. JAMA, 2108. Медицина внутренних органов, 2019; Cicardi M, et al. HAWK под патронатом EAACI. Классификация, диагностика и подход к лечению ангионевротического отека: консенсусный отчет Международной рабочей группы по наследственному ангионевротическому отеку. Аллергия, 2014; Отани И.М., Банерджи А. Приобретенный дефицит ингибитора С1. Клиники иммунологии и аллергии Северной Америки, 2017; Lewis LM, et al. Экаллантид для неотложного лечения ангионевротического отека, индуцированного ингибитором ангиотензинпревращающего фермента: многоцентровое рандомизированное контролируемое исследование. Анналы неотложной медицины, 2015; Валериева А. и др. Рекомбинантный
