Отеки при пороках сердца у детей
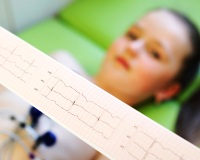
Сердечная недостаточность у детей возникает при врожденных кардиоваскулярных пороках, воспалительных (кардиты) и невоспалительных (кардиомиопатии) болезнях, поражении миокарда вследствие системных заболеваний, генетических синдромов. Ключевые симптомы — одышка в покое и при нагрузке, отеки нижних конечностей, повышенная утомляемость. В диагностическом поиске используются инструментальные методики (ЭхоКГ, ЭКГ, рентгенография грудной клетки), клинические и биохимические анализы крови. Лечение проводится медикаментозно (кардиотоники, ингибиторы АПФ, β-блокаторы), при сердечных пороках показана хирургическая коррекция.
Общие сведения
Сердечная недостаточность (СН) является клиническим синдромом, ее признаки встречаются при разных кардиоваскулярных патологиях и поражении других органов у детей. В структуре общей летальности в детских стационарах кардиальные заболевания занимают 26%, и сердечной недостаточности принадлежит среди них первое место. Это значимая проблема в современной детской кардиологии, которая ведет к снижению качества жизни и инвалидизации больных. Патологию разграничивают с диагнозом «недостаточность кровообращения», который отражает полиэтиологические изменения и обычно не связан с поражением сердца.

Сердечная недостаточность у детей
Причины
Признаки сердечной недостаточности отмечаются при нарушении сократительной способности миокарда при его прямом или опосредованном повреждении. Этиологическая структура зависит от возраста ребенка. Основные причины заболевания у новорожденных — врожденные сердечные пороки, гипоксическое поражение миокарда в перинатальном периоде. У детей старшего возраста кардиальная недостаточность возникает под действием различных факторов, основными из которых служат:
- Органические болезни сердца. Чаще всего патология становится следствием воспалительных процессов — эндокардита, миокардита, перикардита. У детей причиной сердечной недостаточности зачастую выступают дилатационная и гипертрофическая формы кардиомиопатии.
- Нарушения ритма и проводимости. У детей преимущественно встречаются непароксизмальные и пароксизмальные желудочковые тахикардии, полные атриовентрикулярные блокады, предсердные или желудочковые экстрасистолы. К редким причинам относят синдром Вольфа-Паркинсона-Уайта.
- Острая ревматическая лихорадка. Ревматизм вызывает нарушение сердечной функции у подростков. Заболевание обусловлено повреждением клапанного аппарата и нарушениями гемодинамики. Клинические симптомы несостоятельности миокарда развиваются после одного приступа ревматической лихорадки.
- Внесердечные патологии. Среди причин сердечной недостаточности повышается удельный вес системных поражений соединительной ткани и васкулитов. Изредка признаки СН встречаются при нервно-мышечных заболеваниях, митохондриальных болезнях и генетических синдромах.
Патогенез
В развитии сердечной недостаточности у детей выделяют базовые патофизиологические механизмы, которые запускаются независимо от этиологических факторов заболевания. На начальном этапе поражения миокарда включаются компенсаторные процессы. Повышаются частота сердечных сокращений, периферическое сосудистое сопротивление. Полость левого желудочка сердца расширяется, а его стенка гипертрофируется. Чем старше ребенок, тем активнее у него работают адаптационные механизмы.
По мере истощения компенсаторных возможностей организма состояние пациента ухудшается. Существуют три гипотезы нарушения сократимости миокарда: «энергетический голод» кардиомиоцитов, угнетение процессов возбуждения, снижение чувствительности волокон к ионам кальция. В результате сердечные полости расширяются, снижается эффективный выброс крови в систолу.
Далее активизируется ренин-ангиотензин-альдостероновая система, усиливается выделение катехоламинов и предсердного натрийуретического пептида. У детей появляются симптомы нарушения центральной и периферической гемодинамики. При хроническом варианте сердечной недостаточности происходит перестройка иммунной и нейроэндокринной системы, усиливается клеточный апоптоз.
Классификация
Стандартная классификация Нью-Йоркской сердечной ассоциации NYHA не применяется в детском возрасте из-за сложности клинических критериев. По течению СН у детей подразделяют на острую и хроническую форму, по локализации поражения — на левожелудочковую и правожелудочковую. Для хронической сердечной недостаточности существует расширенная классификация, учитывающая симптомы и данные инструментального обследования. Согласно ей выделяют 3 стадии:
- IA — признаки заболевания отсутствуют при физической нагрузке и в покое, однако при кардиологическом обследовании выявляются отклонения результатов от нормы.
- IB — у детей начинаются незначительные симптомы во время физической активности, которые сопровождаются сердечной дисфункцией.
- IIA — клинические признаки болезни сочетаются с изолированными проявлениями лево- или правожелудочковой недостаточности.
- IIB — симптомы наблюдаются при незначительных физических нагрузках или в покое, им сопутствует застой в обоих кругах кровообращения.
- III — тяжелая стадия недостаточности, характеризующаяся необратимыми анатомо-функциональными нарушениями внутренних органов детей.
Симптомы
На клиническую картину сердечной недостаточности влияет возраст больного. У младенцев первые признаки патологии выявляются сразу после рождения. Родители замечают бледность или синюшность кожных покровов, которые наблюдаются постоянно или возникают при кормлении и крике (аналогах физических нагрузок). Появляется одышка, хриплое дыхание. Вследствие кислородного голодания новорожденный становится вялым и сонливым, отказывается от груди или бутылочки.
Основные симптомы расстройства у старших детей включают одышку, слабость, отеки ног. В начале болезни эти признаки проявляются только при умеренной или интенсивной активности, поэтому долгое время остаются незамеченными. Когда патология прогрессирует, чувство нехватки воздуха появляется при неспешной ходьбе, медленном подъеме по ступеням, а на тяжелое течение указывает одышка в состоянии покоя.
Помимо классических проявлений, определяются симптомы, характерные для основного заболевания, вызвавшего сердечную недостаточность. У детей бывает покалывание, жжение или давящие боли в груди слева. Иногда возникают спонтанные обмороки, которым предшествует слабость, головокружение, перебои в работе сердца. На воспалительную этиологию состояния указывает озноб, лихорадка, недомогание.
При острой сердечной недостаточности состояние ухудшается внезапно, часто признаки возникают на фоне полного здоровья. Беспокоят сильная одышка и удушье, ребенок принимает вынужденное положение сидя, облокотившись руками о колени, или лежа с высоко поднятым изголовьем. При дыхании слышны хлюпающие звуки, изо рта выделяется розовая пена. Критические расстройства гемодинамики проявляются потерей сознания.
Осложнения
При сердечной недостаточности у детей нарушается кровоснабжение тканей, что приводит к истощению, замедлению темпов физического и психического развития. Со стороны дыхательной системы возможны застойные пневмонии, гидроторакс, ТЭЛА. К частым осложнениям относят нарушения функций почек (25-30%), тромбоэмболические патологии (до 3,5%), аритмии. Острая СН без лечения заканчивается смертью ребенка от кардиогенного шока или отека легких.
Диагностика
Обследование у детского кардиолога начинается со сбора анамнеза и симптомов. Дети редко жалуются на одышку, но при детальном расспросе оказывается, что пациенту сложно подниматься по лестнице, он избегает активных игр, плохо успевает на уроках физкультуры. При физикальном осмотре выявляют типичные признаки состояния: отеки на ногах, увеличение печени, цианоз. Для окончательной диагностики важную роль играют инструментальные и лабораторные методы:
- Эхокардиография. При УЗИ оценивают сохранность сократительной и насосной функций, работу клапанов и наличие регургитации крови, давление в сердечных камерах. При исследовании у детей обнаруживаются признаки кардиомиопатии, врожденные пороки. Особенности кровотока изучаются с помощью допплерографии.
- ЭКГ. По результатам кардиограммы врач делает заключение об электрической функции сердца, обнаруживает кардиографические симптомы нарушения проводимости и ритма. При недостаточности наблюдается гипертрофия желудочков, которая проявляется на ЭКГ увеличением вольтажа зубцов R в определенных отведениях и отклонением электрической оси сердца.
- Рентгенография ОГК. На обзорной рентгенографии выявляется кардиомегалия или характерные изменения конфигурации сердца, патогномоничные для отдельных врожденных пороков. При развитии острой левожелудочковой недостаточности на снимке обнаруживают признаки отека легких.
- КТ грудной клетки. Исследование проводится как уточняющий метод, если не получено достаточной информации о состоянии кардиоваскулярной системы. КТ показывает детальное строение сердечных камер и крупных сосудов. В диагностике аритмогенной дисплазии желудочков исследование заменяют МРТ.
- Лабораторные анализы. В гемограмме обнаруживают компенсаторно повышенный уровень гемоглобина и эритроцитов. В биохимическом исследовании крови обращают внимание на соотношение плазменных протеинов, уровень рН. По показаниям назначается анализ на миокардиальные маркеры, липидограмма.
Лечение сердечной недостаточности у детей
Консервативная терапия
Сначала врач оценивает клинические симптомы и эхокардиографические признаки СН, устанавливает ее вариант и степень тяжести, чтобы подобрать оптимальную терапевтическую схему. Ребенку не назначают потенциально опасные для прогрессирования болезни препараты (антагонисты кальция, НПВС, кортикостероиды). Для лечения сердечной недостаточности применяются медикаменты следующих групп:
- Кардиотоники. Лекарства улучшают силу и эффективность сердечных сокращений, повышают выброс крови из левого желудочка. Используются сердечные гликозиды и негликозидные кардиотоники.
- Диуретики. Путем снижения объема циркулирующей крови уменьшают нагрузку на желудочки, улучшают центральное и периферическое кровообращение. Эффективны петлевые и калийсберегающие диуретики.
- Ингибиторы АПФ. Основная группа препаратов для фармакотерапии и профилактики сердечной недостаточности, быстро устраняющих ее симптомы. Они действуют на патогенетические механизмы развития болезни, обладают гипотензивным эффектом.
- Бета–блокаторы. Медикаменты улучшают сократительную активность миокарда и доставку кислорода к органу, оказывают антиаритмическое действие. Они снижают прямое токсическое влияние катехоламинов на сердце, ремоделируют диастолическую функцию левого желудочка.
- Кардиометаболические средства. Лекарства, улучшающие кровоснабжение и трофику миокарда, рекомендованы при всех вариантах СН. Они повышают эффективность других препаратов, ускоряют восстановление после воспалительной кардиопатологии.
Хирургическое лечение
Оперативное вмешательство в основном назначают при врожденных пороках, сопровождающихся сердечной недостаточностью. Если выявлены симптомы жизнеугрожающих состояний, операцию делают новорожденным сразу после их рождения. Компенсированные состояния являются показанием к плановой помощи детских хирургов на первом-втором году жизни ребенка. При тяжелых аритмиях устанавливают кардиостимулятор.
Прогноз и профилактика
Вероятность полного выздоровления определяется причинами патологии. Если признаки возникли у детей, страдающих воспалительными кардиальными болезнями или операбельными пороками, ребенка удается полностью вылечить. Менее оптимистичный прогноз для детей, у которых обнаружены симптомы врожденных или хронических прогрессирующих заболеваний, но своевременная терапия значительно улучшает качество жизни. Профилактика сердечной недостаточности — своевременное выявление и терапия кардиологических болезней.
Источник
Врожденные пороки сердца – группа заболеваний, объединенных наличием анатомических дефектов сердца, его клапанного аппарата или сосудов, возникших во внутриутробном периоде, приводящих к изменению внутрисердечной и системной гемодинамики. Проявления врожденного порока сердца зависят от его вида; к наиболее характерным симптомам относятся бледность или синюшность кожных покровов, шумы в сердце, отставание в физическом развитии, признаки дыхательной и сердечной недостаточности. При подозрении на врожденный порок сердца выполняется ЭКГ, ФКГ, рентгенография, ЭхоКГ, катетеризация сердца и аортография, кардиография, МРТ сердца и т. д. Чаще всего при врожденных пороках сердца прибегают к кардиохирургической операции – оперативной коррекции выявленной аномалии.
Общие сведения
Врожденные пороки сердца – весьма обширная и разнородная группа заболеваний сердца и крупных сосудов, сопровождающихся изменением кровотока, перегрузкой и недостаточностью сердца. Частота встречаемости врожденных пороков сердца высока и, по оценке различных авторов, колеблется от 0,8 до 1,2% среди всех новорожденных. Врожденные пороки сердца составляют 10-30% всех врожденных аномалий. В группу врожденных пороков сердца входят как относительно легкие нарушения развития сердца и сосудов, так и тяжелые формы патологии сердца, несовместимые с жизнью.
Многие виды врожденных пороков сердца встречаются не только изолированно, но и в различных сочетаниях друг с другом, что значительно утяжеляет структуру дефекта. Примерно в трети случаев аномалии сердца сочетаются с внесердечными врожденными пороками ЦНС, опорно-двигательного аппарата, ЖКТ, мочеполовой системы и пр.
К наиболее частым вариантам врожденных пороков сердца, встречающимся в кардиологии, относятся дефекты межжелудочковой перегородки (ДМЖП – 20%), дефекты межпредсердной перегородки (ДМПП), стеноз аорты, коарктация аорты, открытый артериальный проток (ОАП), транспозиция крупных магистральных сосудов (ТКС), стеноз легочной артерии (10-15% каждый).
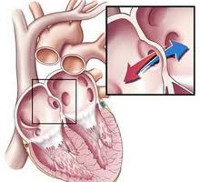
Врожденные пороки сердца
Причины врожденных пороков сердца
Этиология врожденных пороков сердца может быть обусловлена хромосомными нарушениями (5%), генной мутацией (2-3%), влиянием факторов среды (1-2%), полигенно-мультифакториальной предрасположенностью (90%).
Различного рода хромосомные аберрации приводят к количественным и структурным изменениям хромосом. При хромосомных перестройках отмечаются множественные полисистемные аномалии развития, включая врожденные пороки сердца. В случае трисомии аутосом наиболее частыми пороками сердца оказываются дефекты межпредсердной или межжелудочковой перегородок, а также их сочетание; при аномалиях половых хромосом врожденные пороки сердца встречаются реже и представлены, главным образом, коарктацией аорты или дефектом межжелудочковой перегородки.
Врожденные пороки сердца, обусловленные мутациями единичных генов, также в большинстве случаев сочетаются с аномалиями других внутренних органов. В этих случаях сердечные пороки являются частью аутосомно-доминантных (синдромы Марфана, Холта-Орама, Крузона, Нунана и др.), аутосомно-рецессивных синдромов (синдром Картагенера, Карпентера, Робертса, Гурлер и др.) или синдромов, сцепленных с Х-хромосомой (синдромы Гольтца, Аазе, Гунтера и др.).
Среди повреждающих факторов внешней среды к развитию врожденных пороков сердца приводят вирусные заболевания беременной, ионизирующая радиация, некоторые лекарственные препараты, пагубные привычки матери, производственные вредности. Критическим периодом неблагоприятного воздействия на плод являются первые 3 месяца беременности, когда происходит фетальный органогенез.
Внутриутробное поражение плода вирусом краснухи наиболее часто вызывает триаду аномалий – глаукому или катаракту, глухоту, врожденные пороки сердца (тетраду Фалло, транспозицию магистральных сосудов, открытый артериальный проток, общий артериальный ствол, клапанные пороки, стеноз легочной артерии, ДМЖП и др.). Также обычно имеют место микроцефалия, нарушение развития костей черепа и скелета, отставание в умственном и физическом развитии.
Кроме краснухи беременной, опасность для плода в плане развития врожденных пороков сердца представляют ветряная оспа, простой герпес, аденовирусные инфекции, сывороточный гепатит, цитомегалия, микоплазмоз, токсоплазмоз, листериоз, сифилис, туберкулез и др.
В структуру эмбриофетального алкогольного синдрома обычно входят дефекты межжелудочковой и межпредсердной перегородки, открытый артериальный проток. Доказано, что тератогенное действие на сердечно-сосудистую систему плода оказывает прием амфетаминов, приводящий к транспозиции магистральных сосудов и ДМЖП; противосудорожных средств, обусловливающих развитие стеноза аорты и легочной артерии, коарктации аорты, открытого артериального протока, тетрады Фалло, гипоплазии левых отделов сердца; препаратов лития, приводящих к атрезии трехстворчатого клапана, аномалии Эбштейна, ДМПП; прогестагенов, вызывающих тетраду Фалло, другие сложные врожденные пороки сердца.
У женщин, страдающих преддиабетом или диабетом, дети с врожденными пороками сердца рождаются чаще, чем у здоровых матерей. В этом случае у плода обычно формируются ДМЖП или транспозиция крупных сосудов. Вероятность рождения ребенка с врожденным пороком сердца у женщины с ревматизмом составляет 25 %.
Кроме непосредственных причин, выделяют факторы риска формирования аномалий сердца у плода. К ним относят возраст беременной младше 15-17 лет и старше 40 лет, токсикозы I триместра, угрозу самопроизвольного прерывания беременности, эндокринные нарушения у матери, случаи мертворождения в анамнезе, наличие в семье других детей и близких родственников с врожденными пороками сердца.
Классификация врожденных пороков сердца
Существует несколько вариантов классификаций врожденных пороков сердца, в основу которых положен принцип изменения гемодинамики. С учетом влияния порока на легочный кровоток выделяют:
- врожденные пороки сердца с неизмененным (либо незначительно измененным) кровотоком в малом круге кровообращения: атрезия аортального клапана, стеноз аорты, недостаточность легочного клапана, митральные пороки (недостаточность и стеноз клапана), коарктация аорты взрослого типа, трехпредсердное сердце и др.
- врожденные пороки сердца с увеличенным кровотоком в легких: не приводящие к развитию раннего цианоза (открытый артериальный проток, ДМПП, ДМЖП, аортолегочный свищ, коарктация аорты детского типа, синдром Лютамбаше), приводящие к развитию цианоза (атрезия трехстворчатого клапана с большим ДМЖП, открытый артериальный проток с легочной гипертензией)
- врожденные пороки сердца с обедненным кровотоком в легких: не приводящие к развитию цианоза (изолированный стеноз легочной артерии), приводящие к развитию цианоза (сложные пороки сердца – болезнь Фалло, гипоплазия правого желудочка, аномалия Эбштейна)
- комбинированные врожденные пороки сердца, при которых нарушаются анатомические взаимоотношения между крупными сосудами и различными отделами сердца: транспозиция магистральных артерий, общий артериальный ствол, аномалия Тауссиг-Бинга, отхождение аорты и легочного ствола из одного желудочка и пр.
В практической кардиологии используется деление врожденных пороков сердца на 3 группы: пороки «синего» (цианотического) типа с веноартериальным шунтом (триада Фалло, тетрада Фалло, транспозиция магистральных сосудов, атрезия трехстворчатого клапана); пороки «бледного» типа с артериовенозным сбросом (септальные дефекты, открытый артериальный проток); пороки с препятствием на пути выброса крови из желудочков (стенозы аорты и легочной артерии, коарктация аорты).
Нарушения гемодинамики при врожденных пороках сердца
В результате выше названных причин у развивающего плода может нарушаться правильное формирование структур сердца, что выражается в неполном или несвоевременном закрытии перепонок между желудочками и предсердиями, неправильном образовании клапанов, недостаточном повороте первичной сердечной трубки и недоразвитии желудочков, аномальном расположении сосудов и т. д. После рождения у части детей остаются открытыми артериальный проток и овальное окно, которые во внутриутробном периоде функционируют в физиологическом порядке.
Ввиду особенностей антенатальной гемодинамики, кровообращение развивающегося плода при врожденных пороках сердца, как правило, не страдает. Врожденные пороки сердца проявляются у детей сразу после рождения или через какое-то время, что зависит от сроков закрытия сообщения между большим и малым кругами кровообращения, выраженности легочной гипертензии, давления в системе легочной артерии, направления и объема сброса крови, индивидуальных адаптационных и компенсаторных возможностей организма ребенка. Нередко к развитию грубых нарушений гемодинамики при врожденных пороках сердца приводит респираторная инфекция или какое-либо другое заболевание.
При врожденных пороках сердца бледного типа с артериовенозным сбросом вследствие гиперволемии развивается гипертензия малого круга кровообращения; при пороках синего типа с веноартериальным шунтом у больных имеет место гипоксемия.
Около 50% детей с большим сбросом крови в малый круг кровообращения погибают без кардиохирургической помощи на первом году жизни от явлений сердечной недостаточности. У детей, перешагнувших этот критический рубеж, сброс крови в малый круг уменьшается, самочувствие стабилизируется, однако постепенно прогрессируют склеротические процессы в сосудах легких, обусловливая легочную гипертензию.
При цианотических врожденных пороках сердца венозный сброс крови или ее смешение приводит к перегрузке большого и гиповолемии малого круга кровообращения, вызывая снижение насыщения крови кислородом (гипоксемию) и появление синюшности кожи и слизистых. Для улучшения вентиляции и перфузии органов развивается коллатеральная сеть кровообращения, поэтому, несмотря на выраженные нарушения гемодинамики, состояние больного может длительное время оставаться удовлетворительным. По мере истощения компенсаторных механизмов, вследствие длительной гиперфункции миокарда, развиваются тяжелые необратимые дистрофические изменения в сердечной мышце. При цианотических врожденных пороках сердца оперативное вмешательство показано уже в раннем детском возрасте.
Симптомы врожденных пороков сердца
Клинические проявления и течение врожденных пороков сердца определяется видом аномалии, характером нарушений гемодинамики и сроками развития декомпенсации кровообращения.
У новорожденных с цианотическими врожденными пороками сердца отмечается цианоз (синюшность) кожных покровов и слизистых оболочек. Синюшность усиливается при малейшем напряжении: сосании, плаче ребенка. Белые пороки сердца проявляются побледнением кожи, похолоданием конечностей.
Дети с врожденными пороками сердца обычно беспокойные, отказываются от груди, быстро устают в процессе кормления. У них появляется потливость, тахикардия, аритмии, одышка, набухание и пульсация сосудов шеи. При хроническом нарушении кровообращения дети отстают в прибавлении веса, росте и физическом развитии. При врожденных пороках сердца обычно сразу поле рождения выслушиваются сердечные шумы. В дальнейшем обнаруживаются признаки сердечной недостаточности (отеки, кардиомегалия, кардиогенная гипотрофия, гепатомегалия и др.).
Осложнениями врожденных пороков сердца могут стать бактериальный эндокардит, полицитемия, тромбозы периферических сосудов и тромбоэмболии сосудов головного мозга, застойные пневмонии, синкопальные состояния, одышечно-цианотические приступы, стенокардитический синдром или инфаркт миокарда.
Диагностика врожденных пороков сердца
Выявление врожденных пороков сердца осуществляется путем комплексного обследования. При осмотре ребенка отмечают окраску кожных покровов: наличие или отсутствие цианоза, его характер (периферический, генерализованный). При аускультации сердца нередко выявляется изменение (ослабление, усиление или расщепление) сердечных тонов, наличие шумов и пр. Физикальное обследование при подозрении на врожденный порок сердца дополняется инструментальной диагностикой – электрокардиографией (ЭКГ), фонокардиографией (ФКГ), рентгенографией органов грудной клетки, эхокардиографией (ЭхоКГ).
ЭКГ позволяет выявить гипертрофию различных отделов сердца, патологическое отклонение ЭОС, наличие аритмий и нарушений проводимости, что в совокупности с данными других методов клинического обследования позволяет судить о тяжести врожденного порока сердца. С помощью суточного холтеровского ЭКГ-мониторирования обнаруживаются скрытые нарушения ритма и проводимости. Посредством ФКГ более тщательно и детально оценивается характер, длительность и локализация сердечных тонов и шумов. Данные рентгенографии органов грудной клетки дополняют предыдущие методы за счет оценки состояния малого круга кровообращения, расположения, формы и размеров сердца, изменений со стороны других органов (легких, плевры, позвоночника). При проведении ЭхоКГ визуализируются анатомические дефекты перегородок и клапанов сердца, расположение магистральных сосудов, оценивается сократительная способность миокарда.
При сложных врожденных пороках сердца, а также сопутствующей легочной гипертензии, с целью точной анатомической и гемодинамической диагностики, возникает необходимость в выполнении зондирования полостей сердца и ангиокардиографии.
Лечение врожденных пороков сердца
Наиболее сложной проблемой в детской кардиологии является хирургическое лечение врожденных пороков сердца у детей первого года жизни. Большинство операций в раннем детском возрасте выполняется по поводу цианотических врожденных пороков сердца. При отсутствии у новорожденного признаков сердечной недостаточности, умеренной выраженности цианоза операция может быть отложена. Наблюдение за детьми с врожденными пороками сердца осуществляют кардиолог и кардиохирург.
Специфическое лечение в каждом конкретном случае зависит от разновидности и степени тяжести врожденного порока сердца. Операции при врожденных дефектах перегородок сердца (ДМЖП, ДМПП) могут включать пластику или ушивание перегородки, рентгенэндоваскулярную окклюзию дефекта. При наличии выраженной гипоксемии детям с врожденными пороками сердца первым этапом выполняется паллиативное вмешательство, предполагающее наложение различного рода межсистемных анастомозов. Подобная тактика улучшает оксигенацию крови, уменьшает риск осложнений, позволяет провести радикальную коррекцию в более благоприятных условиях. При аортальных пороках выполняется резекция или баллонная дилатация коарктации аорты, пластика аортального стеноза и др. При ОАП производится его перевязка. Лечение стеноза легочной артерии заключается в проведении открытой или эндоваскулярной вальвулопластики и т. д.
Анатомически сложные врожденные пороки сердца, при которых радикальная операция не представляется возможной, требуют выполнения гемодинамической коррекции, т. е. разделения артериального и венозного потоков крови без устранения анатомического дефекта. В этих случаях могут проводиться операции Фонтена, Сеннинга, Мастарда и др. Серьезные пороки, не поддающиеся оперативному лечению, требуют проведения пересадки сердца.
Консервативное лечение врожденных пороков сердца может включать в себя симптоматическую терапию одышечно-цианотических приступов, острой левожелудочковой недостаточности (сердечной астмы, отека легких), хронической сердечной недостаточности, ишемии миокарда, аритмий.
Прогноз и профилактика врожденных пороков сердца
В структуре смертности новорожденных врожденные пороки сердца занимают первое место. Без оказания квалифицированной кардиохирургической помощи в течение первого года жизни погибает 50-75% детей. В периоде компенсации (2-3 года) смертность снижается до 5%. Ранее выявление и коррекция врожденного порока сердца позволяет существенно улучшить прогноз.
Профилактика врожденных пороков сердца требует тщательного планирования беременности, исключения воздействия неблагоприятных факторов на плод, проведения медико-генетического консультирования и разъяснительной работы среди женщин групп риска по рождению детей с сердечной патологией, решения вопроса о пренатальной диагностике порока (УЗИ, биопсия хориона, амниоцентез) и показаниях к прерыванию беременности. Ведение беременности у женщин с врожденными пороками сердца требует повышенного внимания со стороны акушера-гинеколога и кардиолога.
Источник
