Отек сердца у новорожденного

Миокардит у новорожденных чаще всего вызывается вирусами Коксаки В (тип 1–5) и Коксаки А13, может быть проявлением внутриутробного генерализованного воспалительного процесса с полиорганным поражением.
Кардиты могут развиваться в антенатальном и постнатальном периоде. При этом антенатальные кардиты бывают ранние и поздние. При раннем антенатальном кардите у плода к концу внутриутробного развития воспалительный процесс в сердце заканчивается, после рождения у ребенка обычно диагностируется кардиопатия, причем преобладают фибросклеротические процессы. Поэтому т. н. ранние врожденные кардиты отождествляются с понятием фиброэластоз. Фиброэластоз рассматривают как неспецифическую морфологическую реакцию эндокарда на любой миокардиальный стресс. В качестве такого стресса могут выступать врожденные пороки сердца, гипоксия, инфекции, кардиомиопатии. Если повреждающий агент (бактерии, вирусы) действует на миокард в последние 2–3 месяца внутриутробного периода, развивается поздний антенатальный кардит (возникает в последнем триместре беременности или в момент рождения ребенка). В миокарде возникает классическое воспаление, что соответствует термину «миокардит», и младенцы рождаются с острой фазой воспаления и клиническими проявлениями заболевания. Острый постнатальный кардит развивается у детей в периоде новорожденности, он может быть врожденным и приобретенным. Для позднего антенатального и острого постнатального кардита характерно увеличение размеров сердца и гипертрофия миокарда. Все перечисленные варианты повреждения миокарда имеют особенности, обусловленные этиологическими факторами.
Классификация миокардитов предусматривает прежде всего разделение их по этиологическому признаку. Данный подход к классификации миокардитов осуществлен в МКБ-10. Общепринятых патогенетических принципов классификации миокардитов нет. Традиционно по патогенетическому признаку можно выделять 3 формы миокардитов:
- инфекционные и инфекционно-токсические – при гриппе, энтеровирусной инфекции и др.;
- аллергические (иммунные) – при системных заболеваниях, инфекционно-аллергический миокардит, лекарственный, сывороточный;
- токсико-аллергические – при тиреотоксикозе, уремии.
По распространенности процесса различают очаговые миокардиты и диффузные миокардиты.
По течению: острые миокардиты, подострые миокардиты, рецидивирующие миокардиты, хронические миокардиты, абортивные миокардиты.
Диагноз «миокардит» у новорожденных может основываться на рекомендациях Нью-Йоркской кардиологической ассоциации (New York Heart Association – NYHA), разработанных в 1973 г., 1979 г., дополненных M. Take и соавт. (1981) и Ю. К. Новиковым (1988).
Для диагностики острого диффузного миокардита используют две группы диагностических критериев – «больших» и «малых» симптомов.
Диагноз «миокардит» ставится на основании наличия хронологической связи признаков перенесенной инфекции (аллергии, токсического воздействия и т. п.) с двумя «большими» критериями миокардита или сочетание одного «большого» с двумя «малыми» критериями.
«Большие» критерии – имеется хронологическая связь перенесенной инфекции (или аллергической реакции, или токсического воздействия) с появлением следующих кардиальных симптомов:
- кардиомегалия;
- сердечная недостаточность;
- кардиогенный шок;
- синдром Морганьи–Адамса–Стокса;
- патологические изменения на ЭКГ, в том числе сердечные аритмии и нарушения проводимости;
- повышение активности кардиоспецифических ферментов (КФК, МВ-КФК, ЛДГ 1 и ЛДГ 2) и содержания тропонинов.
«Малые» критерии:
- лабораторное подтверждение перенесенной инфекции (например, высокие титры противовирусных антител);
- ослабление I тона;
- протодиастолический ритм галопа.
Осложнения миокардитов:
- острая сердечная недостаточность (сердечная астма, отек легких);
- пароксизмальные нарушения ритма с сердечной недостаточностью;
- АВ-блокада с остановкой сердца;
- перикардит;
- развитие дилатационной кардиомиопатии.
Диагностика миокардита
Целью диагностики является подтверждение наличия миокардита, установление его этиологии, степени тяжести заболевания для назначения необходимой терапии, определение клинического варианта течения заболевания и выявление наличия осложнений. В клинической практике используются комплексные методы диагностики.
При изучении материнского и акушерско-гинекологического анамнеза устанавливается связь кардиальной симптоматики у новорожденного с эпизодами персистирующего инфекционного процесса у матери во время беременности (респираторно-вирусные и бактериальные инфекции, гипертермия неясного генеза), связь поражения сердца у новорожденного с заболеваниями матери.
Данные физикального обследования от близких к норме до признаков тяжелой сердечной дисфункции. В легких случаях могут выглядеть без признаков интоксикации, чаще всего наблюдается тахикардия и тахипноэ. При более тяжелых формах наблюдаются признаки циркуляторной недостаточности левого желудочка. При широком распространении воспаления выявляются классические симптомы сердечной дисфункции, такие как набухание шейных вен, крепитация в основаниях легких, асцит, периферические отеки, выслушивается третий тон или ритм галопа, что может отмечаться при вовлечении в патологический процесс обоих желудочков.
При аускультации сердца выраженность первого тона может быть снижена. Шумы митральной и трикуспидальной регургитации свидетельствуют о дилятации желудочка. Диффузное воспаление может привести к развитию перикардиального выпота, без тампонады, что проявляется шумами трения.
Клинический анализ крови: при легкой форме общий анализ крови существенно не изменяется. При миокардите средней степени тяжести и тяжелом отмечается повышение СОЭ, умеренное увеличение количества лейкоцитов с нейтрофилезом и палочкоядерным сдвигом, моноцитозом. Наиболее выраженный лейкоцитоз и токсическая зернистость нейтрофилов характерны для бактериальных миокардитов. Вирусные миокардиты далеко не всегда сопровождаются лейкоцитозом даже при выраженной симптоматике.
Клинический анализ мочи, как правило, без изменений. При развитии выраженной сердечной недостаточности в моче обнаруживаются белок, цилиндры (преимущественно гиалиновые). В биохимическом анализе крови определяется повышенный уровень белков острой фазы (С-реактивный белок), увеличивается содержание в крови фибрина, гаптоглобина, серомукоида, снижается содержание альбуминов.
Ревматологический скрининг проводится для исключения системных воспалительных заболеваний (антистрептолизин-0, ревматоидный фактор, антинуклеарные антитела и антитела к
2-спиральной ДНК, LE-клетки).
При определении сердечных ферментов отмечается повышение активности МВ-креатинфосфокиназы и сердечных тропонинов – I и T.
Для подтверждения вирусной этиологии необходимо выделить вирус методом ПЦР-диагностики из крови, кала, перикардиальной жидкости, смывов из носоглотки, а также исследовать сыворотку на антитела к вирусам, связывание комплемента и подавление гемагглютинации в острой фазе и в стадии выздоровления. Посев крови на стерильность позволяет определить бактериальную природу заболевания.
Определение титров сывороточных антител при вирусных миокардитах из4за своей низкой специфичности и задержке роста вирусных титров редко используется в клинической практике.
В диагностике миокардита может помочь исследование некоторых иммунных реакций, непосредственно связанных с поражением миокардиальных волокон. Можно выявить увеличение титра противомиокардиальных антител, торможение миграции лейкоцитов при постановке реакции с антигенами миокарда и миокардиальных мембран. Реакция торможения миграции лейкоцитов (индекс миграции) указывает на наличие сенсибилизации лейкоцитов к данному антигену. Наличие аутоиммунных сдвигов существенно помогает диагностике миокардитов, в патогенезе которых иммунный механизм играет ведущую роль. Обнаружение этих реакций, в особенности в сочетании с гиперферментемией существенно помогает в дифференциации миокардита тяжелого течения и дилатационной кардиомиопатии. Сложность такой дифференциации обусловливается еще и тем, что, по данным эндомиокардиальной биопсии, через 1–2 месяца после начала болезни при условии проведения современной противовоспалительной терапии в биоптатах не удается обнаружить признаков воспалительного процесса.
М. С. Суровикина и соавт. продемонстрировали важную роль в патогенезе миокардита нарушений калликреин-кининовой системы, что коррелирует с тяжестью течения болезни. Наиболее тяжелому течению миокардита соответствует более выраженное усиление активности кининогенеза, резкое повышение адсорбции калликреина на каолине, резкое снижение активности ингибиторов калликреина. При более легком течении эти сдвиги выражены в меньшей степени. Отмечается также, что при рецидивах миокардита одновременно наблюдаются сдвиги калликреин-кининовой системы, мало выраженные в период ремиссии болезни.
Цитохимическое исследование лейкоцитов крови у больных миокардитами выявляет выраженные изменения клеточного метаболизма, обнаружена активация щелочной фосфатазы нейтрофилов. Повышение активности нейтрофилов при инфекционно-аллергическом миокардите следует рассматривать как результат выброса в кровь молодых, функционально активных нейтрофилов для осуществления ими защитных реакций (показатель активности патологического процесса). При изучении метаболизма лимфоцитов у больных инфекционно-аллергическими миокардитами отмечено отчетливое повышение активности кислой фосфатазы в лимфоцитах, при этом повышение кислой фосфатазы может сочетаться как с нормальным уровнем сукцинатдегидрогеназы, так и с ее снижением. Последнее сочетание рассматривается как показатель наличия аллергических реакций замедленного типа.
Приведенные данные вселяют оптимизм в отношении возможности улучшения диагностики миокардита. Перечисленные лабораторные показатели еще не вошли в широкую практику, однако сам факт дальнейших изысканий тех или иных сдвигов свидетельствует о необходимости иметь в арсенале врача дополнительные диагностические критерии.
При рентгенологическом исследовании грудной клетки размеры сердца варьируют от нормальных до значительно увеличенных.
При легком течении миокардита размеры сердца не изменены. При миокардите средней степени тяжести и тяжелой форме размеры сердца значительно увеличены, при выраженной кардиомегалии сердце как бы расплывается на диафрагме, дуги его сглаживаются, пульсация ослабевает. В легких можно обнаружить умеренно выраженный венозный застой, широкие корни (может отмечаться их смазанность, нечеткость), усиление венозного рисунка.
При электрокардиографии часто обнаруживают изменения интервала ST и зубца Т, нарушения ритма и проводимости. Характерны неспецифические изменения – синусовая тахикардия, могут наблюдаться блокады (атриовентрикулярная блокада – блокада правой ветви с или без блокады обоих пучков, полная блокада или задержка внутрижелудочковой проводимости), желудочковая аритмия вплоть до фибрилляции, изменения амплитуды желудочкового комплекса. Изменения в зубце Т, интервале ST, схожие с таковыми при миокардиальной ишемии или перикардита (псевдоинфарктная картина).
При эхокардиографии обнаруживают расширение желудочков и снижение сократимости миокарда, иногда – выпот в полость перикарда. Эхокардиография проводится для исключения других причин сердечной декомпенсации (например, клапанных, врожденных, амилоидоза) и определения степени сердечной дисфункции (обычно диффузная гипокинезия и диастолическая дисфункция). Эхокардиография также позволяет локализовать «воспалительный участок» (нарушения движения стенок, истончение стенок, перикардиальный выпот). Биопсия миокарда – проводится правожелудочковая эндомиокардиальная биопсия. Это стандартный критерий для диагностики миокардита несмотря на то, что он несколько ограничен в чувствительности и специфичности, так как воспаление может быть распространенным или очаговым. Биопсия миокарда подтверждает диагноз «миокардит», но редко бывает полезна для выбора методов лечения, большая зависимость результата от интерпретации данных также служит причиной ложноположительных или ложноотрицательных результатов. Поскольку этот метод связан со взятием образцов, его чувствительность повышается при многократной биопсии (при однократной биопсии высока частота ложноотрицательных результатов). Частота ложноположительных результатов достаточно высока, благодаря небольшому числу лимфоцитов, в норме присутствующих в миокарде, и трудностям при дифференцировке лимфоцитов и других клеток (таких как эозинофилы при эозинофильном эндокардите).
На основании перечисленных методов диагностики диагноз «миокардит» у новорожденного ребенка можно выставить на основании характерных для него признаков: четкой связи с перенесенной инфекцией; лабораторных признаков воспаления, повышения в крови уровня кардиоспецифических ферментов (МВ-фракция креатинфосфокиназы, тропонинов), кардиомегалии и эхокардиографических признаков нарушения сократительной функции миокарда левого желудочка, клинических проявлений недостаточности кровообращения.
=================
Вы читаете тему:
Дифференциальная диагностика поражений миокарда инфекционного и гипоксического генеза у новорожденных детей
1. 4 варианта постгипоксического синдрома дезадаптации сердечно-сосудистой системы.
2. Миокардит у новорожденных: формы, критерии, диагностика.
3. Постгипоксическая дисфункция миокарда у новорожденных.
Лашина Н. Б. Республиканский научно-практический центр «Мать и дитя».
Опубликовано: “Медицинская панорама” № 8, ноябрь 2010.
Источник
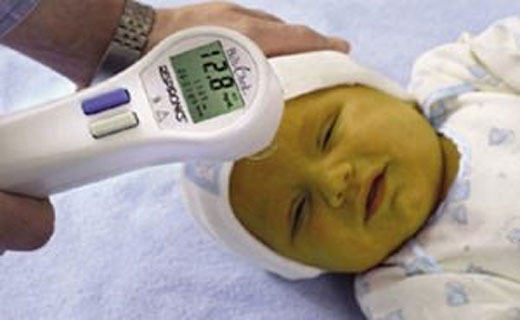
Практически каждому взрослому известно явление, которое встречается и у детей: отеки у новорожденных нередко отмечаются врачами как симптомы разных заболеваний. Причиной таковых является накопление жидкости. Это происходит в различных клетках и тканях, а также в подкожном слое, что приводит к образованию припухлостей. Локализация и распространение отеков может быть разной, что и заставляет докторов пристально наблюдать за малышами.
Симптомы и диагностика
Отеки, которые очевидны, — это припухлости, которые могут иметь самую разную локализацию и площадь. Как правило, при обнаружении таких симптомов врачи назначают комплекс анализов, среди которых не только общие исследования, но и рентген, посевы, УЗИ. По завершению обследования определяется направление лечения, но в первую очередь, крохе назначают диуретические медикаменты, которые помогают вывести лишнюю жидкость.
Но есть и скрытые отеки – головного мозга, кишечника, легких. Такие состояния являются патологическими и достаточно опасными, поэтому требует незамедлительного вмешательства докторов.

Следует отметить, что новорожденный рождается с определенной отечностью из-за соответствующего предлежания в утробе матери. Если же вполне обычные отеки не проходят, значит, пора искать более серьезную причину. Например, отеки, которые проявляются в области суставов, могут свидетельствовать об остеомиелите, а в области брюшной стенки – о перитоните. Припухлости около стоп могут говорить о нарушении оттока лимфы или о синдроме Тернера. Поэтому наличие отеков – причина для внимательного наблюдения.
Скрытые отеки чаще всего проявляются вместе с множеством других симптомов, которые говорят о серьезных проблемах, поэтому требуют неотложной помощи.
Причины отеков

Отеки у новорожденных возникают по самым разнообразным причинам, как, впрочем, и у взрослых. Но такие симптомы у детей могут говорить о довольно серьезных заболеваниях и нарушениях.
Обширный отек возникает из гормональных нарушений, инфекционной болезни, нарушения обменных процессов, почечная и сердечная недостаточность.
Локальные накопления жидкости являются признаками таких проблем:
- гематомы, венозный застой, переломы, передавливание отдельных частей тела, нарушения в работе лимфатической системы;
- повреждения эпидермиса – например, перегрев, переохлаждение, ожоги;
- инфекции, которые приводят к поражениям кожи;
- аллергия;
- сердечная недостаточность.
Все вышеперечисленные отеки у новорожденных являются приобретенными, но есть категория и врожденных проблем:
- нарушения кровообращения;
- анемия;
- поражения мозга;
- внутриутробные инфекции;
- аномалии развития внутренних органов;
- наследственные заболевания разного характера;
- некроз почечных канальцев, который может развиваться из-за обвития пуповиной;
- гипотериоз;
- синдром Тернера;
- красная волчанка, сахарный диабет, гестоз, многоводие, перенесенные матерью.
Лечение отеков у младенцев
Как уже говорилось, в первую очередь проводят терапию, которая помогает вывести лишнюю жидкость из организма, улучшить отток лимфы и кровообращение. Как правило, диуретики назначают в течение 1-3 дней и прекращают их давать, если грудничок выглядит намного лучше и отечность сходит.
Сложнее проводить лечение, когда малышу назначили инфузионную терапию – введение растворов самого разного назначения, которые сами по себе увеличивают количество жидкости в организме крохи. Отказаться от таковой невозможно, если малыш родился раньше срока или его состояние требует оказания незамедлительной помощи. В этом случае все равно назначают диуретики, а объемы лекарственных растворов уменьшают.
Отеки – симптом довольно серьезный, поэтому игнорировать его не просто нельзя, но и следует обязательно показать доктору. Как правило, проявляются такие признаки заболеваний сразу после рождения, но особенно важно вовремя заметить те припухлости или общие симптомы, которые возникают на 3-4 день жизни крохи. Своевременно начатое лечение позволит устранить осложнение и наиболее адекватно восстановить состояние новорожденного.
Источник

Отеки у новорожденных образуются за счет избыточного накопления жидкости в организме, которая способна скапливаться в подкожной клетчатке, в мышцах и в полостях тела. Отекание бывает и у взрослых людей, и у детей, и у новорожденных. Отеки бывают местные, то есть те, которые ограничены определенной областью тела, и генерализованные – те, которые распространены довольно широко. У новорожденных деток, если, например, сравнить содержание уровня жидкости в подкожной клетчатке и самой коже и общий объем жидкостей тела, то он буде в несколько раз больше, чем у взрослого человека.
Лечение отеков у новорожденных
Диагностика и лечение отеков
Отеки у новорожденных – это своеобразные припухлость кожи, в некоторых случаях с изменением цвета. Если появились отеки у новорожденного, то для того, чтобы подтвердить диагноз и определить тактику лечения, малышу проводят такие обследования, как: анализ крови, посевы на наличие инфекции, ультразвуковое обследование, рентген. Лечение отеков у новорожденных направлено на устранение причины появления отеков и по возможности в ограничении количества жидкости, которая вливается. Грудному ребенку также для лечения отека назначаются диуретические препараты, которые способствуют выведению лишней жидкости из организма.

Причины отеков у новорожденных
Генерализованный отек у новорожденного может быть приобретенным. Также причиной отека у новорожденных могут быть гормональный криз, тяжелое инфекционное заболевание, неадекватная инфузионная терапия, некоторые гормональные нарушения, нарушение обмена веществ, сердечная или почечная недостаточность.
Каковы основные причины отеков?
Причины, по которым образуются местные отеки у новорожденных, могут быть такие:
- нарушение оттока лимфы по причине сдавливания части тела, гематомы, переломы, пороки, связанные с развитием лимфатической системы, венозный застой;
- травматические повреждения кожи, например, химические ожоги, переохлаждение, перегрев или механические повреждения;
- присутствие инфекции, способной вызывать отек подкожной клетчатки или кожи над местом поражения;
- аллергические реакции, сердечная недостаточность и отдельные заболевания, связанные с наследственностью;
Факторами, которые вызывают отеки у новорожденных и ведут к появлению водянки (врожденный генерализованный отек), являются:
- гемолитические болезни новорожденных, гемолитическая анемия;
- постгеморрагическая анемия;
- поражения мозга;
- опухоли;
- инфекции;
- патологии структуры сердца, почек, легких, лимфатических и кровеносных сосудов, заболевания костей и желудка;
- наследственные заболевания, связанные с обменом веществ;
- хромосомные аномалии;
- патологические процессы у матери, например, гестоз, сахарный диабет, красная волчанка и другие.
Теперь вам известны основные причины отеков у новорожденных и методы их лечения.
В данном обзоре мы поговорим о таких вопросах, как отек головного мозга, последствия данного заболевания. Отечностью головного мозга называют возрастание его габаритов по причине скапливания жидкости в пределах межклеточного пространства. Возрастание объема мозга по причине интрацеллюлярной жидкости называют набуханием. Если говорить о патофизиологии, эти состояния (набухание и отечность) часто могут развиваться обоюдно и переходить взаимно друг в друга, потому с клинической точки зрения данные понятия можно толковать в качестве отечность мозга.
Лечение отека головного мозга
Как проводится лечение отека головного мозга?
В случае устойчивой гипертензии для лечения отека головного мозга можно посоветовать регулярный люмбальный дренаж (с помощью тонкой полиэтиленовой трубки), который вводится согласно методике, напоминающей катетеризацию кровеносного ствола по Сельдингеру.
В случае умеренной или нормальной гипертензии (около 140 мм) достаточно для лечения мозга у новорожденного провести эвакуацию ликвора, ввести внутривенно глюкозу 40% (100 мл). При повышенном давлении ликвора включают в дегидратационный комплекс осмотические диуретики: мацнитол (60-80 г), мочевина (30-40 г), а кроме того лазикс (около 40 г). В осложненных ситуациях их используют два-три раза в день. Менее действенными в лечении являются гипертонические растворы на основе глюкозы, ртутные диуретики, CaC12 (10% – около 200 мл).
Беспричинное обширное использование диуретиков при лечении отека мозга у новорожденного серьезного действия может спровоцировать обезвоживание и большие потери кальция, а ведь травме мозга сопутствует достаточно высокая склонность к утрате данного электролита. Обязательным при отеке головного мозга является каждодневный контроль за ЭКГ, ионограммой, диурезом, водным балансом в общем и распределением воды по главным секторам.
Причины отека мозга у новорожденного
Каковы причины появления отека головного мозга?
Отек головного мозга можно отнести к вторичным признакам повреждения. Она может быть локальной или генерализованной. Отек головного мозга появляется у новорожденного при разнообразных болезнях, которые поражают нервную систему: инсульт, черепно-мозговая травма, абсцесс и опухоли головного мозга, менингиты и энцефалиты, гипоксия, разные формы окклюзионной гидроцефалии, разные синдромы ухудшения осмотического равновесия, общие интоксикации, заражения, ожоги тела, злокачественная гипертоническая болезнь и т.д. В клинике и эксперименте доказано, что разные этиологические факторы провоцируют патогенетические разнообразные формы отечности мозга у новорожденного, однако механизмы его увеличения равноценны.
Последствия отека головного мозга
Какими могут быть последствия отека головного мозга?
Последствия такого отека могут быть разными, т.к. отек мозга может быть вызван у новорожденных родовой травмой. В качестве предрасполагающих факторов отека головного мозга могут рассматриваться болезни матери, а также токсикозы беременных, в случае которых развивается у мамы и плода гипоксия.
Прогнозирование последующего развития ребенка с отеком головного мозга, характеризуется как полным излечением, либо развитием незначительных ухудшений ЦНС, так и очень тяжелыми болезнями, которые нуждаются в обязательной терапии и наблюдении у невропатологов.
Главными вариантами последствий перинатального повреждения ЦНС и детей в раннем возрасте являются полное излечение, задержание моторного, психического, либо речевого развития детей, синдром ухудшения внимательности с гиперактивностью, разнообразные невротические реакции, эпилепсия, синдром вегетативно-висцеральной дисфункции, детский церебральный паралич, гидроцефалия и т.д.
После терапии в неврологическом отделении ребенок подлежит совместному диспансерному наблюдению невропатологом, педиатром, а в некоторых ситуациях и психиатром.
Источник
