Отек руки при меланоме

Отеки – частое осложнение распространенного рака, кроме того у любого онкологического больного могут быть и другие причины для развития отечного синдрома, существенно усугубляющие состояние и усиливающие отечность тканей. Особенность отеков при раке в их устойчивости к лечению и нередкое тяжелое течение с выраженным болевым синдромом.
Виды отёков при раке
Отеки при раке, а точнее отечный синдром, обусловленный выходом жидкости из сосудистого русла и длительной задержкой в тканях, может быть симметричным или генерализованным и локальным, с преимущественным поражением отдельной анатомической части.
К генерализованному варианту относится скопление жидкости во внутренних полостях организма – асцит или плеврит, а также перикардит – жидкость в сердечной сорочке.
Такое тяжелое и характерное для терминальных сердечных заболеваний состояние общей отечности организма, как анасарка, при раке встречается нечасто, тем не менее при раковой кахексии жировая клетчатка больного раком способна незаметно впитать до 5 литров «лишней» жидкости, формируя скрытый отечный синдром. У человека без истощения можно заметить избыточное скопление уже 2 литров межтканевой жидкости, при распространенном раке и сниженной активности заметить увеличение объема весьма непросто.
Локальные отеки при злокачественных процессах практически всегда не воспалительного характера, а обусловлены блокировкой оттока межтканевой жидкости по лимфатическим сосудам.
Причины отёков при раке
Отечность формируется при разбалансировке процесса выхода питающей клетки плазмы из кровеносного русла в ткани, откуда она почти полностью, но уже в «отработанном виде», должна всасываться венозными капиллярами. В норме только десятая часть жидкости задерживается в межклеточном пространстве и впоследствии уходит в лимфатическое русло.
При большинстве злокачественных процессов баланс нарушает недостаточное функционирование лимфатического коллектора, когда сосуды и лимфоузлы забиваются клетками рака, а опухолевые конгломераты лимфатических узлов перестают «качать» лимфу. Подобный механизм формирования отечности вплоть до слоновости возникает при неоперабельном раке шейки матки с метастазами в паховые и тазовые лимфоузлы. Аналогичное происходит при оперированном раке молочной железы с лимфедемой – лимфостазом, когда полностью удаляются подмышечные лимфоузлы, и при неоперабельном раке груди с метастатическими регионарными лимфоузлами, не только не функционирующими, но и дополнительно сдавливающими крупные сосуды.
Часто лимфатическую недостаточность усугубляет сдавление вены конгломератом опухолевых лимфоузлов и её тромбоз – сопряженное с распространенным злокачественным процессом нарушение свертывающей системы крови. Резко выраженный отек головы и шеи развивается при синдроме верхней полой вены, когда нарушает венозный отток быстро растущая в средостении злокачественная опухоль. Аналогичный механизм включается при поражении печени метастазами рака и увеличении органа до гигантского размера – во всю брюшную полость.
Нечасто встречающаяся паранеопластическая нефропатия, сопровождающая развитие злокачественного процесса с высокой потребностью в белке L-аспарагине, напрямую повреждает почечные клубочки, что ведет к потерям белков и развитию генерализованных отеков.
Механизм отёка при раковом истощении
При кахексии у онкологических пациентов механизм формирования «голодных» отеков обусловлен снижением концентрации циркулирующих в крови белков. Гипопротеинемия приводит к массированному выходу плазмы в межклеточное пространство, что автоматически сопровождается снижением артериального давления и, в свою очередь, включением компенсаторного механизма его повышения. Повышение сосудистого давления опять ведет к выведению жидкой части крови в интерстициальное пространство и ещё большей отечности тканей. Подобным образом формируются отеки при заболеваниях почек, осложненных почечной недостаточностью, циррозе печени с исходом в печеночную недостаточность.
В терминальной стадии рака недостаточность питания пациента сопряжена с падением функциональных возможностей печеночных клеток, не синтезирующих достаточного количества белков, и дополняется высочайшей потребностью раковых клеток в энергии за счёт «обкрадывания» всех остальных тканей организма. То есть формируется порочный круг, когда при недостаточном печеночном синтезе и низком поступлении извне белок усилено сжигается клетками рака.
Избыток жидкости в тканях при недостатке объема циркулирующей плазмы вынуждает организм к выбросу гормонов и биологически активных веществ, поддерживающих артериальное давление, что ещё больше подрывает сердечно-сосудистую и дыхательную систему, ухудшая состояние больного раком.
Скрытые отеки и анасарка при раковой кахексии требуют активных лечебных мероприятий, только капельницами с белковыми растворами удалить их невозможно. Необходимы активные и незамедлительные действия по купированию патологических реакций, которые специалисты Клиники выполняют по индивидуально разработанной и патогенетически ориентированной лечебной программе.
Диагностика и клинические симптомы
При раке диагностика отека несложна – это утолщение и изменение кожи, которая становится теплее или холоднее, при надавливании надолго остается ямочка.
При прогрессирующем ухудшении самочувствия и тяжести состояния у истощенного пациента отмечается быстрая и необъяснимая диетическим режимом прибавка в весе нескольких килограмм. Ткани утолщаются, по консистенции напоминая мягкое тесто.
Наиболее просто выявляется несимметричный лимфатический отек, типичный признак – отечность тыла стопы или кисти по типу подушки, когда невозможно собрать кожу в складочку. Сила тяжести приводит к застою жидкости сначала в нижних отделах, постепенно захватывая всю конечность снизу-вверх. При прогрессировании лимфатического отека конечность приобретает синюшный цвет с мраморными разводами, мягкие ткани значительно уплотняются и раздуваются, все это сопровождается нарастанием болевого синдрома и ограничением движений.
Отек конечности вследствие блокады оттока метастазами в паховой или подмышечно-надключичной лимфатической группе, нарастает очень быстро без тенденции к регрессии даже при максимально щадящем режиме и постоянном возвышенном положении. Конечность приобретает гигантский объем с мраморно-синюшной растрескивающейся кожей. Малейшее движение приводит к сильнейшей боли, купировать которую крайне сложно. Пациенты жалуются, что конечность распирает изнутри, и опасаются, что «может лопнуть». Сдавление сосудов отечными мышцами приводит к вторичному тромбозу вен, что усугубляет страдания пациента и чревато миграцией тромботических масс в легочные сосуды с угрозой смерти.
При синдроме верхней полой вены отек тканей буквально сдавливает верхние дыхательные пути и сосуды шеи. Язык и губы увеличиваются в размере, нередки точечные кровоизлияния в конъюнктиве глаза и ухудшение зрения. Беспокоит постоянная головная боль, при повороте головы возможен глубокий обморок. Состояние быстро ухудшается, присоединяется тяжелая легочно-сердечная недостаточность, возможна смерть из-за разрыва мозгового сосуда.
При раке любой отек прогрессивно ухудшает состояние за счёт декомпенсации сердечно-сосудистой и дыхательной системы, из-за застоя в легких и неадекватности газообмена в тканях развивается полиорганная недостаточность.
С отечным синдромом любой выраженности у онкологического пациента невозможно справиться только мочегонными препаратами, лечение отеков при раке требует комплексных мероприятий, в том числе с использованием специального оборудования и реанимационных техник, и обязательно мультицисциплинарной команды специалистов: онколога, кардиолога, реаниматолога, нутрициолога, нефролога. У врачей клиники большой опыт паллиативной помощи, в том числе успешной борьбы с тяжелыми отеками.
Список литературы:
- Суворова Г.Ю., Мартынов А.И. /Отёчный синдром: клиническая картина, дифференциальная диагностика, лечение // М.: ГЭОТАР-Медиа; 2009.
- Либис, Р.А., Лискова Ю.В./ Дифференциальная диагностика отечного синдрома: учебное пособие // Оренбург: Изд-во ОрГМА, 2011.
- López-Novoa J.M., Rodríguez-Peña A.B., Ortiz A. et al./Etiopathology of chronic tubular, glomerular and renovascular nephropathies: clinical implications // J. Transl. Med.; 2011, Vol. 9.
- Moore K.P., Wong F., Gines P. et al. /The management of ascites in cirrhosis: report on the consensus conference of the International Ascites Club // Hepatology; 2003, Vol. 38. № 1.
Источник

Меланома (от греческого melanos – черный) – это злокачественная опухоль, происходящая из меланоцитов. Это осоые клетки, которые преимущественно локализуются в дерме и синтезируют пигмент меланин. Его количество определяет цвет кожи.
Больше всего таких клеток содержится в пигментных невусах, в народе называемыми родинками. Однако определенное количество меланоцитов имеется в слизистых оболочках внутренних и наружных органов, а также в глазном яблоке. Соответственно, опухоль может развиваться в любом из них.
Почему развивается меланома
Ответа на вопрос, почему происходит злокачественная трансформация меланоцитов и развивается меланома, нет. Однако установлены факторы риска, при наличии которых вероятность развития опухоли увеличивается:
- 1-2 фототип кожи – это люди со светлой кожей, светлыми или рыжими волосами.
- Частые солнечные ожоги, особенно в детском и юношеском возрасте.
- Длительное пребывание на солнце.
- Наличие меланомы у близких родственников.
- Наличие более 100 родинок на теле, либо большое количество родимых пятен (50) у людей младше 20 лет.
- Меланоз Дюбрея.
- Генетическая предрасположенность.
- Гормональные перестройки – половое созревание, климакс.
Большое значение имеет травматизация родинок, в ряде случаев для того чтобы развилась меланома, достаточно травмировать пигментный невус 1-2 раза. Нужно иметь ввиду, что травматизация может носить хронический характер. Например, родимые пятна часто травмируются одеждой при расположении на шее, в паховых складках, на туловище.
Как проявляется меланома
Симптомы меланомы очень разнообразны. Она может иметь разные размеры, форму, цвет и поверхность. Размеры варьируют от 1-2 мм до нескольких сантиметров, форма может быть самой различной. Что касается цвета, то здесь тоже имеются варианты. Чаще всего меланома черная, но может быть коричневой, фиолетовой или даже розовой. Нередки случаи, когда в одном новообразовании сочетается сразу несколько цветов.
Поверхность меланомы может быть неизмененной, но со временем она может изъязвляться, кровоточить или мокнуть. На начальной стадии характерен симптом лаковой кожи, когда на опухоли отсутствует кожный рисунок.
С точки зрения клинических проявлений выделяют следующие формы меланомы:
- Поверхностно-распространяющаяся меланома. Сначала она выглядит как коричневое или черное пятно или бляшка, если она и возвышается над поверхностью кожи, то незначительно. В таком состоянии она может находиться до 7 лет. При прогрессировании она утолщается и превращается в узел, при этом может изменяться ее окрас
- Узловая меланома. Имеет форму узла, полипа или гриба, синекрасного или черного цвета. Постепенно его поверхность изъязвляется и начинает кровоточить.
- Лентиго-меланома. Является результатом злокачественного перерождения меланоза Дюррея. Длительное время (до 20 лет) она существует в виде пятна или бляшки, а затем начинается ее вертикальный рост. При этом, очаг принимает неправильную форму и неравномерное окрашивание.
- Акральная меланома. Она развивается на пальцах руки или ног в ногтевом ложе и имеет вид темного пятна под ногтем.
Стадии
- 0 стадия, или меланома in situ – имеется дисплазия или неизвазивное поражение злокачественными клетками.
- 1 стадия – толщина меланомы составляет не более 1 мм, или до 2 мм но без изъязвления поверхности.
- Вторая стадия выставляется, если толщина изъязвленной опухоли более составляет более 2 мм, или менее 2 мм при отсутствии изъязвления ее поверхности.
- 3 стадия выставляется если меланома дает метастазы в регионарные лимфатические узлы.
- 4 стадия – любая меланома с метастазами во внутренние органы.
Как диагностируется меланома
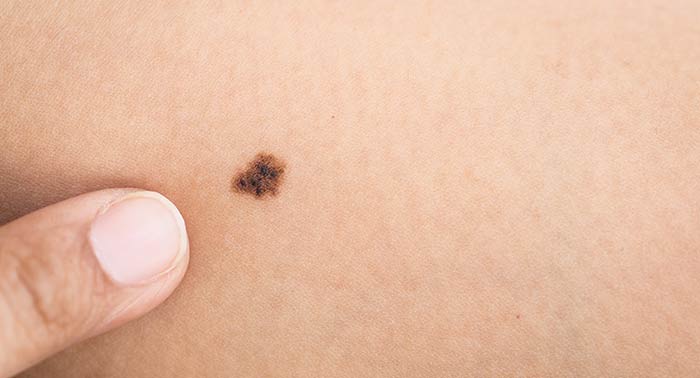
Несмотря на то, что меланома, как правило, располагается на кожных покровах и доступна осмотру, поставить диагноз на начальных стадиях не всегда представляется возможным. Большое значение уделяется самоосмотру кожных покровов, при этом особое внимание необходимо уделить невусам. Заподозрить злокачественное новообразование можно по следующим признакам:
- Асимметричность.
- Неровность и нечеткость края родинки.
- Неравномерность окраски.
- Диаметр родинки более 6 мм.
- Наличие ряда характерных изменений невуса: изменение пигментации (усиление или наоборот, ослабление), изменение кожного рисунка (гладкость поверхности невуса или наоборот, ее шелушение или изъязвление), появление покраснения вокруг родинки, зуд, чувство жжения или покалывания. Сюда же относится и исчезновение родимого пятна.
При наличии этих признаков рекомендуется обратиться к дерматологу. Он проведет физикальный осмотр с помощью дерматоскопии (изучит новообразование под 10-40 кратным увеличением) и когерентной томографии.
Во время приема осматривается кожа всего тела, в том числе голова и кожа подошв стоп. Это необходимо, поскольку есть риск первично-множественных синхронных опухолей, которые диагностируются у 5-10% больных. Причем, это может быть как вторая меланома, так и рак кожи.
Если на поверхности новообразования есть язвы, можно взять мазки-отпечатки и провести цитологическое исследование. Оно позволит поставить диагноз до операции и сразу спланировать радикальное удаление опухоли.
При поиске метастазов выполняется следующее обследование:
- Рентген органов грудной клетки.
- УЗИ.
- Если есть данные за поражения скелета, проводят рентген костей или остеосцинтиграфию.
- Если есть неврологическая симптоматика, выполняют КТ или МРТ.
При увеличении регионарных лимфатических узлов, проводят их пункцию под контролем УЗИ. Данная процедура позволит обнаружить регионарные метастазы.
Если вышеперечисленными методами невозможно подтвердить или опровергнуть диагноз, допускается проведение эксцизионной биопсии с отступом 0,5 см в пределах здоровых тканей с последующим срочным гистологическим исследованием. При подтверждении диагноза, немедленно выполняют радикальную операцию.
Лечение меланомы
Выбор тактики лечения определяется стадией заболевания. При 1-3 стадии основным методом является хирургическая операция, которая по показаниям может дополняться химиотерапией. При 4 распространенных стадиях показана иммунотерапия с учетом молекулярного профиля опухоли. Если такое лечение невозможно, проводят химиотерапию.
Лечение 1-2 стадии
Основным моментом при лечении 1-2 стадии меланомы является радикальное хирургическое удаление опухоли. Ее обязательно удаляют в пределах здоровых тканей, причем величина отступа определяется данными морфологического исследования:
- При меланоме in situ отступают 0.5 см.
- Если по данным гистологического исследования опухоль более 2 мм, рекомендуют отступать от ее края не менее, чем на 1 см.
- При толщине меланомы более 2 мм, отступ должен составлять не менее 2 см.
Допускается уменьшение отступа при удалении меланомы на пальцах рук, чтобы сохранить их функциональность. Если использовалась эксцизионная биопсия, и диагноз был подтвержден, проводят иссечение рубца с вышеуказанными отступами в сроки 4-8 недель.
Рутинное профилактическое удаление регионарных лимфатических узлов или их облучение не показано. Вместо этого проводят биопсию сторожевого ЛУ. Только если ее результаты положительны, проводят лимфаденэктомию.
Лечение распространенных форм заболевания
Лечение больных с распространенными формами меланомы будут зависеть от возможности хирургического удаления опухоли.
Если меланома находится в резектабельном состоянии, рекомендуют ее радикальное удаление с выполнением регионарной лимфаденэктомии. Если при биопсии сторожевого узла были обнаружены метастазы, проводят полное удаление лимфатических узлов подмышечной области с максимально полным удалением жировой клетчатки, в которых эти узлы располагались.
После операции пациенту предлагают проведение иммунотерапии и лучевой терапии на зону регионарного метастазирования. ЛТ снижает вероятность регионарного рецидива у больных с факторами высокого риска:
- Поражение 4 и более ЛУ.
- Если метастаз вышел за пределы капсулы ЛУ.
Облучение проводят в режиме фракционирования в суммарной очаговой дозе 48Гр.
Пациентам с высокими и промежуточными рисками прогрессирования меланомы предлагают проведение адъювантной (послеоперационной) иммунотерапии. В группу риска входят больные со следующими характеристиками меланомы:
- Толщина опухоли от 2 до 4 мм с изъязвленной поверхностью новообразования.
- Толщина опухоли более 4 мм с любой поверхностью.
В рамках адъювантной иммунотерапии применяют препараты рекомбинантного интерферона и блокаторы рецептора CTLA4 (ипилимумаб). Данное лечение увеличивает медиану безрецидивной выживаемости и общей продолжительности жизни. Адъювантная иммунотерапия начинается не позднее 9 недель после операции и продолжается до 12 месяцев.

Лечение нерезектабельной и метастатической меланомы
Лечение нерезектабельных и метастатических форм меланомы определяется молекулярно-генетическими особенностями опухоли. Первоочередное значение имеет наличие мутации в гене BRAF. Если результат теста отрицательный (мутации нет), проводят исследование на мутацию в гене CKIT.
Лечение меланомы при наличии мутации BRAF
В рамках терапии первой линии используется один из следующих методов лечения:
- Монотерапия ингибиторами
- Монотерапия анти-
- Комбинированное применение ингибиторов BRAF+ антиPD
- Комбинированное применение ингибиторов BRAF+ МЕК (для пациентов со стремительным прогрессированием или большим объемом опухолевой массы).
Лечение проводят длительно, до прогрессирования или развития тяжелых осложнений, требующих отмены препаратов. Если молекулярно-генетический статус опухоли не уточнен, назначение данных препаратов не проводится, поскольку есть вероятность парадоксального ускорения и прогрессирования роста меланомы
Также данные препараты могут спровоцировать развитие рака кожи. Поэтому необходимо регулярно осматривать кожные покровы на предмет наличия подозрительных новообразований. Если таковые имеются, их подвергают хирургической обработке. Отмену лечения или уменьшение дозы препаратов при этом не проводят.
Лечение при наличии мутации CKIT
В рамках терапии первой линии, используется терапия анти-PD1 или иматиниб (ингибитор CKIT). Терапия применяется до прогрессирования или развития осложнений, требующих отмены препарата.
При прогрессировании заболевания, при наличии мутаций BRAF и CKIT, в рамках терапии второй линии используются ниволумаб или пембролизумаб. При медленном прогрессировании применяется ингибитор CTLA4 ипилимумаб. При невозможности проведения иммунотерапии используются цитостатики.
Следует отметить, что химиотерапия менее эффективна при лечении меланомы и дает больше осложнений. Поэтому ее не рекомендуют применять в рамках терапии первой линии и используют только тогда, когда все ресурсы исчерпаны или другое лечение недоступно.
Лечение при отсутствии мутаций BRAF и CKIT
При отсутствии данных мутаций, показано назначение ингибиторов PD1. Если опухоль оказалась к ним нечувствительна, или наступило прогрессирование, переходят на ингибиторы CTLA4 (ипилимумаб). В рамках терапии 3 линии применяются цитостатики.
При лечении нерезектабельной меланомы руки может быть применена гипертермическая перфузия с мелфаланом. Этот метод применяется в рамках паллиативной терапии для сохранения конечности у пациентов, не ответивших на иммунотерапию и цитостатическую терапию.
Профилактика меланомы
- Поскольку меланома часто развивается из родинок, рекомендуется проводить регулярный самоосмотр кожных покровов на предмет изменения имеющихся невусов и отслеживание возникновения новых.
- При наличии большого количества родинок, рекомендуется отказаться от загара и нахождения под прямыми солнечными лучами.
- При загаре необходимо пользоваться солнцезащитными средствами.
- Избегать попадания на незащищенную кожу прямых солнечных лучей.
Источник
