Отек мозга и легких у младенца

Отек головного мозга у новорожденных детей – нередкое явление. Как правило, причинами являются инфекционные и неинфекционные заболевания, нарушения развития, родовая травма, особенности прохождения головки ребенка через родовые каналы матери. Опасность состояния в его стертых проявлениях: часто при отеке мозга у младенцев, и так неспособных рассказать о своем самочувствии, наблюдается стертая симптоматика. При этом последствия отека головного мозга могут быть значительными.
Причины и виды отека головного мозга новорожденных
В период новорожденности отек головного мозга наблюдается по причине врожденных и приобретенных заболеваний, сопровождающихся стремительным развитием, родовой травмы. Разделяют отеки мозга инфекционной и неинфекционной этиологии.
При отеках отмечается увеличение количества внутримозговой жидкости, что вызывает изменения в поведении ребенка и определенную симптоматику неврологического характера.
В зависимости от площади поражения выделяют два вида отеков головного мозга.
- Локальный отек
Локальный или региональный отек головного мозга захватывает часть головного мозга, в которой наблюдается патологический процесс или развитие новообразования. Патология или процесс, провоцирующие отечность области мозга, находятся непосредственно в ткани мозга. Наиболее частой причиной считается гематома, возникающая при патологиях родовой деятельности, нарушениях родового процесса, несоответствия размера головки ребенка тазовым костям, а также при послеродовых травмах головы. Причиной регионального отека у детей также может быть наличие кистозных включений в тканях мозга, формирование абсцесса, патологии развития и т. п.
- Генерализованный отек
Генерализованный отек распространяется на всю площадь головного мозга. Причиной могут быть значительные черепно-мозговые травмы, нейроинфекции, интоксикация, асфиксия в родах, а также затруднение оттока ликвора из тканей мозга вследствие травм спинного канала или нарушений развития.
Симптомы отека головного мозга у детей и диагностика состояния
Отек головного мозга и нарастание внутричерепного давления обуславливают ущемление, сдавливание продолговатого мозга, отвечающего за процессы терморегуляции, дыхания, функционирование сердечно-сосудистой системы. Нарушения работы продолговатого мозга приводят к недостаточности функционирования основных жизнеобеспечивающих систем организма ребенка, что провоцирует спектр симптомов и проявлений различной степени тяжести, от незначительных до летального исхода.
Новорожденный ребенок с проявлениями состояния отека головного мозга может длительно и пронзительно плакать, находиться в возбужденном состоянии, иметь нарушения сна. В зависимости от степени тяжести состояния отмечается набухание, выпячивание кожного покрова над мембраной, закрывающей роднички, частые срыгивания, рвота, гипертермия тела (повышенная температура), конвульсии. Дети постарше реагируют потерей сознания, судорожными явлениями. Симптомы локального отека мозга в начале развития или в невыраженной стадии должны дифференцироваться от проявлений других болезней, нарушений и физиологических состояний, в том числе от проявлений младенческих колик.
Диагностика проводится общими и инструментальными методами. Первичная диагностика, определяющая необходимость углубленного изучения, осуществляется врачом-педиатром или неврологом. В нее входят:
- сбор анамнеза о течении беременности матери, особенностях родоразрешения, наличия наследственных заболеваний у ближайших родственников ребенка;
- общий осмотр ребенка врачом, изучение состояния в динамике;
- неврологическое обследование на наличие с степень развитости безусловных рефлексов;
- оценка поведенческих реакций детей;
- анализ психомоторных функций.
Инструментальные методы обследования проводятся после первичной диагностики по назначению специалиста. Могут применяться такие методики, как ультразвуковое исследование, электроэнцефалография, нейросонография, компьютерная томография и так далее, в зависимости от вида нарушения состояния и возраста ребенка.
Лечение и последствия отека мозга у ребенка
Отек мозга относится к категории состояний, требующих неотложной медицинской помощи. Выявление причины патологического процесса и лечение должны начинаться незамедлительно. Важным базисом эффективной терапии отека является диагностика причины нарушения и ее устранение.
Для снятия симптомов отечности используют несколько групп препаратов. В основном прибегают к помощи осмотических диуретиков (Фуросемида, Маннитола, Лазикса) и препаратов группы глюкокортикостероидов.
При неэффективности медикаментов прибегают к хирургическим методам лечения: шунтированию, формированию дополнительных каналов для оттока жидкости, устранению патологии, кисты, образования, провоцирующих скопление ликвора в мозгу.
В зависимости от выраженности симптомов, локализации отека, времени и эффективности терапии, а также от возраста ребенка последствия состояния могут быть как невыраженными, так и приводить к инвалидизации и потере здоровья.
К незначительным последствиям относят временную возбудимость, раздражительность, астеничность. Ребенок даже после выздоровления может проявлять некоторую неврологическую симптоматику: сухожильные рефлексы, рефлекс Бабинского могут проявляться вне возрастных рамок, может наблюдаться повышенный мышечный тонус, односторонний или двухсторонний, некоторая задержка психомоторного развития, нарушения сна, головные боли, укачивание в машине, острая реакция на духоту, шум, яркий счет, резкие запахи и иные раздражители, частые срыгивания.
Дети отличаются высокой пластичностью тканей, поэтому при незначительных осложнениях отека мозга можно рассчитывать на самостоятельную коррекцию последствий.
К более тяжелым состояниям, вызываемым скоплением жидкости в тканях мозга, относят задержку развития у детей в различных областях генеза, интеллектуальные нарушения, дефицит внимания, гиперактивность.
Ребенок после отека мозга может страдать от детского церебрального паралича, эпилептических приступов. Вследствие повышенного внутричерепного давления и раскрытия родничков может наблюдаться увеличение объема головы, гидроцефалия.
Наиболее тяжелое осложнение – перивентикулярная лейкомаляция, некроз тканей головного мозга, возникающий как следствие внутриутробной или родовой гипоксии. Чаще всего страдают дети, родившиеся ранее положенного срока, из-за несформированной системы мозгового кровообращения.
Отек головного мозга – тяжелое состояние, которое требует срочной консультации и терапии. Ребенок, проявляющий даже незначительные симптомы отечности мозга, нуждается в осмотре врача и диагностике причин. Дети, которые начинают получать лечение на ранних сроках развития патологического процесса, имеют намного больше шансов на полное выздоровление без последствий для психики и физиологии.
Источник
Симптомы отека головного мозга у ребенка
- Распирающая головная боль, выраженная приблизительно одинаково во всех областях головы (затылочная, теменная, височная, лобная).
- Тошнота, рвота, не приносящая облегчения.
- Снижение остроты зрения.
- Слабость, сонливость.
- Нарушение сознания вплоть до его полного отсутствия – при этом человек не сразу отвечает на вопросы (или не отвечает вовсе), сонлив, может не открывать глаза даже при болевом раздражении (надавливание на надглазничные дуги).
- Судорожные припадки – непроизвольные сокращения мышц рук и ног, иногда с потерей сознания и прикусыванием языка.
- Нарушение дыхания при сдавлении жизненно важных систем.
Причины отека головного мозга у ребенка
Отек головного мозга является универсальной реакцией на большинство повреждающих воздействий. Поэтому его причиной может быть множество факторов:
- нарушение мозгового кровообращения (инсульт);
- черепно-мозговая травма (ушиб головного мозга);
- опухоли головного мозга;
- отравления (например: угарным газом, лекарственными препаратами);
- тяжелые инфекционные заболевания (клещевой энцефалит (заболевание, передающееся через укусы клещей рода Ixodes и проявляющееся слабостью в конечностях и выраженной интоксикацией), грипп (вирусное заболевание, поражающее дыхательную систему и проявляющееся выраженной интоксикацией));
- хирургические вмешательства на головном мозге.
LookMedBook напоминает: что данный материал размещен исключительно в ознакомительных целях и не заменяет консультацию врача!
Диагностика отека головного мозга у ребенка
- Анализ жалоб и анамнеза заболевания.
- Как давно появились подобные жалобы (головная боль, слабость, сонливость).
- Предшествовало ли какое-то событие появлению указанных жалоб:
- травма головы;
- появление признаков неврологической патологии (слабость в руках и ногах, асимметрия лица, нечленораздельность речи);
- нейрохирургическая операция, отравление (угарным газом).
- Неврологический осмотр: оценка уровня сознания (насколько активно пациент вступает в речевой контакт, открывает ли глаза по команде или на болевой раздражение), а также поиск признаков неврологических нарушений (слабость в конечностях, асимметрия лица, косоглазие), имеющих первичное значение в сравнении с признаками отека головного мозга.
- Осмотр глазного дна: при отеке головного мозга наблюдается отек диска зрительного нерва с нечеткостью его границ.
- Измерение внутричерепного давления – для этого в полость желудочков головного мозга или в его ткань устанавливается специальный датчик, измеряющий давление.
- Люмбальная пункция: с помощью специальной иглы делается пункция (прокол) субарахноидального пространства спинного мозга на поясничном уровне (через кожу спины). В случае отека головного мозга, а значит повышения внутричерепного давления, ликвор (цереброспинальная жидкость, обеспечивающая питание и обмен веществ в головном мозге) вытекает под давлением, иногда струей.
- КТ (компьютерная томография) и МРТ (магнитно-резонансная томография) головы: позволяет послойно изучить строение головного мозга и определить признаки отека головного мозга (уменьшение пространства между мозгом и костями черепа, сдавление и деформация желудочковой системы).
- Возможна также консультация детского нейрохирурга.
Лечение отека головного мозга у ребенка
Нехирургические методы.
- Дегидратация – введение больших доз препаратов, выводящих жидкость из организма (диуретики): гормональные препараты – улучшают функцию гематоэнцефалического барьера (специальная система, ограничивающая поступление некоторых веществ в ткань головного мозга), уменьшают проницаемость сосудов головного мозга.
- Противосудорожные препараты – при возникновении судорог.
Хирургические методы: декомпрессивная краниотомия (открытие полости черепа с формированием дефекта костей черепа – при этом резко снижается давление внутри полости черепа).
Также проводится лечение заболевания, вызвавшего отек головного мозга:
- нарушение мозгового кровообращения – коррекция артериального (кровяного) давления, препараты, улучшающие питание головного мозга (нейротрофики), улучшающие текучесть крови (антиагреганты);
- черепно-мозговая травма – удаление скопления крови, разрушенной ткани мозга;
- опухоли головного мозга – удаление опухоли;
- отравления – дезинтоксикация (удаление токсина из крови);
- тяжелые инфекционные заболевания – антибактериальная и противовирусная терапия.
Осложнения и последствия отека головного мозга у ребенка
- Дислокационный синдром – при этом часть мозга ущемляется внутри полости черепа относительно неподвижных образований (серп мозга, намет мозжечка), что приводит к выраженным неврологическим нарушениям (полное отсутствие сознания, нарушение ритма дыхания, падение артериального (кровяного) давления).
- Риск летального исхода.
Профилактика отека головного мозга у ребенка
Профилактика развития отека головного мозга обычно несостоятельна, так как он развивается вторично, на фоне других тяжелых заболеваний.
Имеет смысл проводить следующие мероприятия:
- учет вводимой жидкости у пациентов, находящихся на лечении;
- профилактическое применение гормональных препаратов (улучшение функций гематоэнцефалического барьера (специальная система, ограничивающая поступление некоторых веществ в ткань головного мозга), уменьшение проницаемости сосудов головного мозга).
Источник
Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Нарушение кровообращения в сосудистой системе головного мозга ребенка сразу после его рождения, вызывающее недостаток кислорода в крови (гипоксемию), определяется как церебральная ишемия у новорожденных. Код по МКБ-10 – P91.0.
Поскольку ишемия, гипоксемия и гипоксия (кислородное голодание) физиологически взаимосвязаны (притом что развитие гипоксии может быть и при нормальном церебральном кровотоке), критическое состояние дефицита кислорода для мозга новорожденных в неврологии считается клиническим синдромом и называется неонатальной гипоксически-ишемической энцефалопатией, развивающейся в течение 12-36 часов после родов.
[1], [2], [3], [4], [5], [6], [7]
Эпидемиология
В неонатальной неврологии и педиатрии эпидемиология клинических проявлений церебральной ишемии у новорожденных отдельно от синдрома гипоксически-ишемической энцефалопатии не фиксируется, поэтому оценка заболеваемости из-за отсутствия критериев их дифференциации проблематична.
Частота неонатальных энцефалопатий, связанных с уменьшением мозгового кровотока и гипоксией мозга, оценивается в 2,7-3,3% случаев на одну тысячу живорожденных детей. При этом 5% детей с младенческими патологиями мозга перенесли его перинатальный инсульт (диагностируется один случай на 4,5-5 тыс. младенцев с патологией церебральной гемодинамики).
Частота перинатальной асфиксии оценивается от одного до шести случаев на тысячу доношенных новорожденных и от двух до десяти случаев у недоношенных. Глобальная оценка имеет большие расхождения: по одним данным, асфиксия новорожденных ежегодно вызывает 840 тыс. или 23% случаев смерти новорожденных во всем мире, а согласно данным ВОЗ – не менее 4 млн., что составляет 38% всех летальных случаев среди детей в возрасте до пяти лет.
Эксперты американской Академии педиатрии пришли к выводу, что наилучшей оценкой частоты неонатальной патологии головного мозга являются данные по численности населения: в среднем три случая на каждую тысячу человек. Согласно мнению некоторых западных нейрофизиологов, те или иные последствия перенесенной при рождении гипоксически-ишемической энцефалопатии наблюдаются у 30% населения развитых стран и более чем у половины жителей развивающихся стран.
[8], [9], [10], [11], [12], [13], [14], [15]
Причины церебральной ишемии у новорожденных
Мозг нуждается в постоянном притоке крови, несущей кислород; у младенцев мозг составляет до 10% массы тела, имеет разветвленную сосудистую систему и потребляет пятую часть кислорода, поступающего с кровью ко всем тканям организма. При снижении церебральной перфузии и оксигенации ткани мозга теряют источник поддержания жизни своих клеток, и известные на сегодняшний день причины церебральной ишемии у новорожденных достаточно многочисленны. Это может быть:
- гипоксемия матери из-за недостаточной вентиляции легких при сердечно-сосудистых заболеваниях, хронической дыхательной недостаточности или пневмонии;
- снижение притока крови к мозгу плода и гипоксемия/гипоксия вследствие плацентарных нарушений, включая тромбоз, отслойку и инфекции плаценты;
- длительное пережатие пуповины во время родов, приводящее к тяжелому метаболическому ацидозу пуповинной крови, системному снижению объема циркулирующей крови (гиповолемии), падению АД и нарушению перфузии головного мозга;
- острое нарушение мозговой гемодинамики (перинатальный или неонатальный инсульт), которое случается у плода с 20-й недели беременности, а у новорожденного – в течение четырех недель после появления на свет;
- отсутствие автоматической саморегуляции церебрального кровотока у недоношенных младенцев;
- нарушение внутриутробного кровообращения плода из-за сужения легочной артерии или врожденных кардиологических аномалий (левосторонней гипоплазии сердца, незаращения Боталлова протока, транспозиции магистральных сосудов и т.д.).
[16], [17], [18], [19], [20], [21], [22]
Факторы риска
Также существуют многочисленные факторы риска развития церебральной ишемии у новорожденных, среди которых невропатологи и гинекологи-акушеры отмечают:
- первую беременность в возрасте старше 35-ти лет или младше 18-ти;
- длительную терапию бесплодия;
- недостаточную массу тела новорожденного (менее 1,5-1,7 кг);
- преждевременные роды (ранее 37-й недели беременности) или переношенная беременность (более 42 недель);
- спонтанный разрыв плодных оболочек;
- слишком долгие или стремительные роды;
- неправильное предлежание плода;
- предлежание сосудов пуповины (vasa previa), чаще всего наблюдаемое при экстракорпоральном оплодотворении;
- травмы черепа младенца во время родов (как результат акушерских ошибок);
- экстренно проведенное кесарево сечение;
- тяжелое кровотечение во время родов;
- наличие у беременной сердечно-сосудистых или аутоиммунных заболеваний, анемии, сахарного диабета, функциональных нарушений щитовидной железы, нарушений свертывания крови (тромбофилии), антифосфолипидного синдрома, инфекционно-воспалительных заболеваний органов малого таза;
- тяжелую артериальную гипотензию в период беременности и поздний гестоз.
Факторами риска мозговой ишемии у младенцев также признаны врожденные патологии крови, связанные с мутациями генов протромбина, тромбоцитарных факторов свертывания крови V и VIII, гомоцистеина плазмы крови, а также ДВС-синдром и полицитемия.
[23], [24], [25], [26], [27], [28], [29]
Патогенез
Церебральная ишемия у новорожденных нарушает метаболизм клеток головного мозга, что приводит к необратимому разрушению структуры нервной ткани и ее дисфункции. В первую очередь, патогенез развития деструктивных процессов связывают со стремительным падением уровня аденозинтрифосфата (АТФ) – главного поставщика энергии для всех биохимических процессов.
Для нормальной функции нейронов также важен баланс между внутриклеточной и внеклеточной концентрацией ионов, мигрирующих через их мембраны. При кислородном голодании мозга в нейронах нарушается трансмембранный градиент ионов калия (К+) и натрия (Na+), а внеклеточная концентрация К+ возрастает, приводя к прогрессирующей аноксидной деполяризации. Одновременно увеличивается приток ионов кальция (Ca2+), инициирующий высвобождение нейромедиатора глутамата, который воздействует на NMDA-рецепторы мозга; их чрезмерная стимуляция (эксайтотоксичность) приводит к морфологическим и структурным изменениям в головном мозге.
Также повышается активность гидролитических ферментов, которые расщепляют нуклеиновые кислоты клеток и вызывают их аутолиз. При этом основание нуклеиновых кислот – гипоксантин – трансформируется в мочевую кислоту, ускоряя образование свободных радикалов (активных форм кислорода и оксида азота) и других соединений, токсичных для мозга. Антиоксидантные защитные механизмы мозга новорожденных еще не полностью развиты, и совокупность перечисленных процессов крайне негативно действуют на его клетки: происходит глиоз нейронов, атрофия глиальных клеток и олигодендроцитов белого вещества.
[30], [31], [32], [33], [34], [35], [36], [37], [38]
Симптомы церебральной ишемии у новорожденных
Клинические симптомы церебральной ишемии у новорожденных и интенсивность их проявления определяются ее видом, степенью тяжести и локализацией зон некроза нейронов.
Виды ишемии включают фокальное или топографически ограниченное повреждение тканей головного мозга, а также глобальное, распространяющееся на многие церебрально-васкулярные структуры.
Первые признаки ишемии мозга при рождении ребенка можно выявить при проверке рефлексов врожденного спинального автоматизма. Но оценка их отклонений от нормы зависит от степени нарушения церебральной перфузии и физиологической зрелости новорожденного.
[39], [40], [41], [42], [43]
Стадии
Так, церебральная ишемия 1 степени у новорожденного (мягкая форма гипоксически-ишемической энцефалопатии) проявляется у доношенного младенца умеренным повышением мышечного тонуса и сухожильных рефлексов (хватательного, Моро и др.). К симптомам также относят избыточное беспокойство с частыми движениями конечностей, постгипоксический миоклонус (подергивания отдельных мышц на фоне мышечной ригидности), проблемы при прикладывании к груди, спонтанно возникающий плач, прерывистый сон.
Если ребенок появился на свет раньше срока, то, кроме снижения безусловных рефлексов (двигательного и сосательного), наблюдается ослабление общего мышечного тонуса в течение первых нескольких дней после рождения. Как правило, это временные аномалии, и, если состояние ЦНС младенца стабилизируется в течение нескольких дней, то ишемия практически не дает неврологических осложнений. Но все зависит от эндогенной регенеративной активности развивающегося мозга конкретного ребенка, а также от выработки церебральных нейротрофинов и факторов роста – эпидермального и инсулиноподобного.
Церебральная ишемия 2 степени у новорожденного (вызывающая умеренно тяжелую форму гипоксически-ишемической энцефалопатии) добавляет к списку уже названных симптомов судороги эпилептического типа; снижение артериального и повышение церебрального давления (наблюдается увеличение и заметное пульсирование родничка); вялость при кормлении и частые срыгивания; проблемы с кишечником; периоды нарушения сердечного ритма и апноэ (замирание дыхания во сне); лабильный цианоз и эффект «мраморной кожи» (из-за вегетососудистых нарушений). Острый период длится примерно в течение десяти суток. Кроме того, неонатологи отмечают возможность осложнений в виде водянки мозга (гидроцефалии), нарушения движений глаз – нистагма, перекоса отклонения глаз (косоглазия).
Если имеется церебральная ишемия 3 степени у новорожденного, то неонатальные рефлексы (сосания, глотания, хватания) отсутствуют, а приступы судорог частые и продолжительные (в течение 24-48 часов после родов). Затем судороги уменьшаются, сменяясь прогрессирующим снижением мышечного тонуса, состоянием ступора, увеличением отека тканей мозга.
В зависимости от локализации основных очагов ишемии мозга могут быть нарушения дыхательной функции (младенец часто требует аппаратной поддержки дыхания); изменения частоты сердечных сокращений; расширение зрачков (плохо реагирующих на свет) и отсутствие глазодвигательного сопряжения («глаза куклы»).
Данные проявления нарастают, что свидетельствует о развитии тяжелой гипоксически-ишемическая энцефалопатии, которая из-за кардиореспираторной недостаточности может завершиться летально.
[44]
Осложнения и последствия
Развитие у новорожденных ишемии головного мозга вызывает индуцированное дефицитом кислорода повреждение его клеток и обусловливает очень серьезные, часто необратимые неврологические последствия и осложнения, которые коррелируются с топографией поражений.
Как показали исследования, ишемии мозга у новорожденных более подвержены пирамидные клетки гиппокампа, клетки Пуркинье в мозжечке, ретикулярные нейроны перироландической области коры головного мозга и вентролатеральной части таламуса, клетки базальных ганглиев, нервные волокна кортикоспинального тракта, ядра среднего мозга, а также нейроны неокортекса и ствола мозга.
У доношенных новорожденных страдают, в первую очередь, кора головного мозга и глубокие ядра, у недоношенных отмечают диффузное разрушение клеток белого вещества полушарий, что обусловливает хроническую инвалидность у выживших детей.
А при глобальной ишемии клеток ствола мозга (в котором сосредоточены центы регуляции дыхания и работы сердца) происходит их тотальная гибель и практически неизбежный летальный исход.
Негативные последствия и осложнения перинатальной и неонатальной ишемии мозга 2-3 степени у детей раннего возраста проявляются эпилепсией, односторонней потерей зрения, задержкой психомоторного развития, двигательными и когнитивными нарушениями, в том числе, детским церебральным параличом. Во многих случаях их выраженность в полной мере может быть оценена к трем годам ребенка.
[45], [46]
Диагностика церебральной ишемии у новорожденных
Начальная диагностика церебральной ишемии у новорожденных осуществляется сразу после родов в ходе стандартного осмотра ребенка и определения так называемого неврологического статуса (по шкале Апгар) – путем проверки степени рефлекторной возбудимости и наличия у него определенных врожденных рефлексов (некоторые из них были упомянуты при описании симптомов данной патологии). Обязательно регистрируются показатели ЧСС и АД.
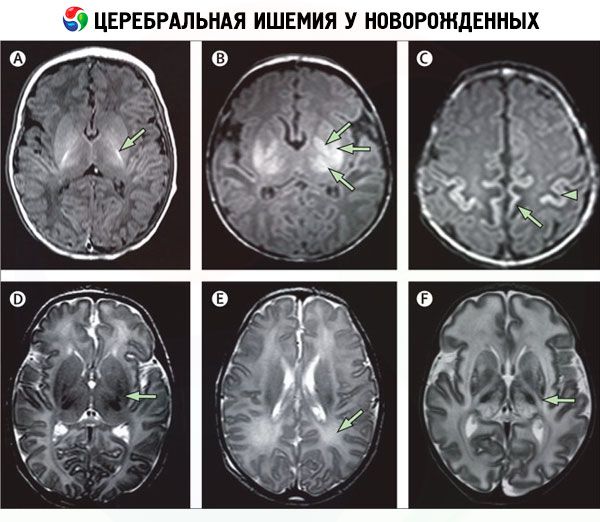
Инструментальная диагностика, особенно неровизуализация, позволяет выявить зоны ишемии головного мозга. С этой целью используют:
- компьютерную томографию церебральных сосудов (КТ-ангиографию);
- магнитно-резонансную томографию (МРТ) головного мозга;
- черепно-мозговое ультразвуковое исследование (УЗИ);
- электроэнцефалографию (ЭЭГ);
- эхокардиографию (ЭКГ).
Лабораторные исследования включают общий клинический анализ крови, а также анализы крови на уровень электролитов, на протромбиновое время и уровень фибриногена, на гематокрит, на содержание газов в артериальной крови; анализ пуповинной или венозной крови на уровень рН (для выявления ацидоза). Также делается анализ мочи – на ее химический состав и осмоляльность.
[47], [48], [49], [50], [51], [52], [53]
Дифференциальная диагностика
Чтобы исключить наличие у младенца перинатального менингоэнцефалита, опухоли мозга, тирозинемии, гомоцистинурии, врожденного синдрома Зеллвегера, нарушения метаболизма пирувата, а также генетически обусловленных митохондриальных нейропатий, метилмалоновой или пропионовой ацидемия, проводится дифференциальная диагностика.
Лечение церебральной ишемии у новорожденных
Во многих случаях на первых этапах лечение церебральной ишемии у новорожденных требует сердечно-легочной реанимации у новорожденных с искусственной вентиляцией легких и всеми мерами по восстановлению гемодинамики сосудистой системы головного мозга, поддержанию гемостаза, а также предупреждению гипертермии, гипо и гипергликемии.
Значительно снижает степень среднего и тяжелого ишемического повреждения клеток головного мозга младенцев контролируемая гипотермия: охлаждение тела на 72 часа до +33-33,5ºC с последующим постепенным доведением температуры до физиологической нормы. Такое лечение не применяется недоношенным детям, родившимся ранее 35-ти недель.
Медикаментозная терапия симптоматическая, например, при тонико-клонических судорогах чаще всего применяются лекарства-антиконвульсанты Дифенин (Фенитоин), Триметин (Триметадион) – дважды в день по 0,05 г (с систематическим мониторингом состава крови).
Для снижения мышечного гипертонуса после трех месяцев в/м может вводиться миорелаксант Толперизон (Мидокалм) – по 5-10 мг на килограмм массы тела (до трех раз в сутки). Препарат может вызвать побочные эффекты в виде тошноты и рвоты, кожных высыпаний и зуда, мышечной слабости, удушья и анафилактического шока.
Улучшению церебральной перфузии способствует капельное внутривенное введение Винпоцетина (дозировка рассчитывается по весу тела).
Для активизации функций головного мозга принято использовать нейропротекторные препараты и ноотропы: Пирацетам (Ноотропил, Нооцефал, Пирроксил, Динацел) – в сутки по 30-50 мг. Сироп Цераксон назначается по 0,5 мл два раза в течение дня. Следует иметь в виду, что этот препарат противопоказан при гипертонусе мышц, а его побочные действия включают аллергическую крапивницу, снижение АД и нарушения сердечного ритма.
При подавлении функций ЦНС применяют Глутан (глутаминовая кислота, Ацидулин) – трижды в сутки по 0,1 г (с контролем состава крови). А препараты-ноотропы гопантеновой кислоты (сироп Пантогам) улучшают оксигенацию тканей головного мозга и проявляют нейропротекторные свойства.
Парентерально применяются витамины В6 (пиридоксина гидрохлорид) и В12 (цианокобаламин) с раствором глюкозы.
Физиотерапевтическое лечение
При легкой степени церебральной ишемии у новорожденного ребенка обязательным является физиотерапевтическое лечение, в частности лечебный массаж, способствующий снижению мышечного гипертонуса. Однако при наличии эпилептического синдрома массаж не применяется.
Улучают состояние новорожденных с ишемией мозга водные процедуры в виде ванна с отваром цветков ромашки аптечной, перечной или лимонной мяты. Лечение травами – см. Успокоительные средства для детей
Профилактика
Невропатологи считают, что профилактика развития у новорожденных синдрома неонатальной гипоксически-ишемической энцефалопатии проблематична. Здесь можно говорить только о надлежащем акушерском сопровождении беременности и своевременном выявлении факторов риска: сердечно-сосудистых патологий у будущей матери, эндокринных нарушений, проблем свертывания крови и т.д. Предупредить влияние анемии, повышенного или пониженного артериального давления или инфекционно-воспалительных заболеваний возможно своевременным лечением. Однако многие проблемы на сегодняшний день доступными средствами неразрешимы.
[54], [55], [56], [57], [58], [59]
Прогноз
Увы, но благоприятный прогноз относительно последствий, к которым приводит церебральная ишемия у новорожденных, отмечается только при ее легкой степени.
Неонатальные энцефалопатии – причина высокого уровня смертности и долгосрочных неврологических патологий у младенцев во всем мире.
[60], [61], [62], [63], [64], [65]
Источник
