Лучевая терапия головного мозга отек
Радиотерапия в лечении злокачественных опухолей – агрессивный метод, который в некоторых случаях является единственно возможным для продления жизни больного. Несмотря на положительный эффект, которого можно добиться при помощи облучения, данная методика характеризуется также проявлением определенных осложнений.
Последствия
Последствия лучевой терапии головного мозга могут быть самыми различными и у каждого онкобольного проявляются различной степенью интенсивности. Специалисты выделяют несколько наиболее часто встречающихся побочных эффектов.
Нарушение состава крови
Иногда после тотального облучения головного мозга отмечается снижение концентрации клеточных структур в костном мозге, которые участвуют в процессе выработки кровяных телец.
По теме
При понижении эритроцитов в составе крови начинает развиваться анемия, что сопровождается усталостью и одышкой. Для устранения данной проблемы специалисты часто проводят переливание крови. При наличии противопоказаний к процедуре назначается эритропоэтин, который вводят в человеческий организм посредством инъекций.
Если отмечается максимальное снижение лейкоцитов, это становится причиной появления нейтропении. В результате риски инфицирования увеличиваются в несколько раз. Для нормализации состояния больного лечение на определенный период приостанавливается.
Усталость
Нередко после радиотерапии при опухолях мозга больной жалуется на повышенную усталость. Это объясняется тем, что после лечения организм направляет все свои силы на восстановление, что было вызвано негативным воздействием облучения на здоровые клетки.
По возможности рекомендуется употреблять до трех литров чистой воды в сутки. Благодаря гидратации организм постепенно восстанавливается.
Степень выраженности усталости будет возрастать по мере проведения терапевтических мероприятий. Данный побочный эффект может не проявляться на начальном этапе радиотерапии, то в конце будет максимально проявляться. Как правило, после облучения пациент ощущает усталость на протяжении 7-14 дней. В некоторых случаях это происходит в течение не одного месяца.
Выпадение волос
Нередким негативным проявлением после лучевой терапии выступает облысение. В случае когда излучением воздействуют на какую-либо определенную область головы, выпадение волосяного покрова будет отмечаться именно в этой зоне. Однако, не исключается проявление такого побочного эффекта и со стороны выхода пучка излучения.
По окончании терапевтического курса волосяные луковицы восстанавливаются, и волосы вновь начинают расти. При этом может возникнуть другая структура, то есть, были кудрявые – стали прямые, цвет, неоднородность, толщина волоска изменится.
Тошнота
Данное осложнение проявляется в основном при воздействии радиационным потоком на нижнюю часть головного мозга. Тошнота может беспокоить на протяжении не одной недели и сопровождаться приступами рвоты.
Для улучшения состояния часто назначается дополнительное лечение, изменяется рацион питания. В большинстве случаев, после окончания курса данный эффект исчезает самостоятельно.
Ухудшение симптомов
В некоторых случаях может отмечаться ухудшение состояния больного на фоне усиления клинической картины, которой сопровождается онкологическое заболевание. При этом нет повода думать о неэффективности лечения и росте злокачественного образования.
Кроме того, в месте обработки под воздействием лучевой терапии возможно развитие отечности, в результате чего давление повышается. Происходит временное ухудшение симптоматики, что сопровождается судорожными приступами, тошнотой и ярко выраженными головными болями.
Для устранения отека назначают, как правило, препараты стероидной группы. При наличии противопоказаний к приему стероидов проводится таргетная терапия – авастин, действие которого способствует понижению внутричерепного давления. При этом развитие кровеносных сосудов, окружающих новообразование, также меняется.
Питание после облучения
Полное восстановление организма невозможно без соблюдения специальной диеты. Кроме того, правильно составленный рацион позволяет снизить выраженность симптоматики болезни и облегчить состояние пациента.
Питание после лучевой терапии подразумевает употребление только полезных продуктов. Чтобы организм начал восстанавливаться, он должен получать большое количество калорий и белка.
Если онкобольной в состоянии сам принимать пищу, то в его рационе в обязательном порядке должны присутствовать сыр, молочная продукция, яйца, бобовые, рыба и мясо. Это основные источники белка. При отсутствии аппетита рекомендуется употреблять высокоэнергетические супы и молочные коктейли.
По теме
Также важно, насколько это возможно, выпивать в день не менее трех литров чистой воды.
При возможных проблемах с питанием можно воспользоваться следующими рекомендациями:
- замена стандартного приема пищи на небольшие перекусы;
- употребление жидких и мягких блюд при затрудненном глотании;
- полный отказ от спиртных напитков, что способствует нарушению работы пищеварительной системы;
- введение в рацион БАДов при необходимости.
Кроме того, если после лучевой терапии у больного имеются определенные сложности с употреблением пищи, то белковую пищу можно заменить на продукты с повышенным содержанием жира.
Несмотря на то что радиотерапия может вызывать появление ряда серьезных побочных эффектов, она все же остается в приоритете у специалистов для лечения рака головного мозга. Как правило, радиационное облучение способствует уничтожению раковых клеток, уменьшению размеров онкологического новообразования, а также уменьшению проявления клинических признаков. Для купирования и контроля нежелательных осложнений применяются различные терапевтические методики.
Источник
Схема лучевой терапии опухоли головного мозга – Европейские рекомендации
Лучевая терапия — лечение заболеваний с использованием ионизирующего излучения. Как правило, применяется при злокачественных заболеваниях, а также при некоторых доброкачественных (например, при макроаденомах гипофиза). В большинстве случаев лучевая терапия опухолей головного мозга проводится в послеоперационном периоде, методом внешнего облучения рентгеновскими лучами. Также используется ряд других методов, таких как интаоперационная лучевая терапия, корпускулярная и брахитерапия. Значение лучевой терапии во многом зависит от радиочувствительности опухоли.
Возможно лечение (например, при медуллобластомах, герминоклеточных опухолях) или продление жизни (например, при глиомах). Цель заключается в обеспечении максимальной или лечебной дозы для опухоли и минимизации повреждения нормальной ткани.
а) Механизм действия. Лучевая терапия проводится избирательно путем концентрации высокой дозы излучения в области опухоли, при этом учитываются различия в резистентности нормальных и раковых тканей. Облучение повреждает ДНК, которая в свою очередь может восстановиться или привести к гибели клеток с помощью различных механизмов. Осознанное управление молекулярными последствиями облучения приводят к ощутимому улучшению результатов.
Чтобы воспользоваться разницей в восстановлении и кинетическом росте в ответ на облучение, суммарная доза делится на малые дозы или «фракции». В принципе при большем количестве фракций можно достигнуть большего эффекта. Таким образом, радикальное лечение сводится к 30 или более фракциям, в то время как паллиативное лечение включает значительно меньше.
б) Стандартное базовое оснащение. Облучение центральной нервной системы (ЦНС) должно выполняться на линейном ускорителе с энергией 4-6 MV. Он должен иметь возможность для структурирования луча и модуляции интенсивности лучевой терапии (МИЛТ). Должны быть доступны современные средства планирования лучевой терапии, основанные на КТ с модулем имитации и проверки луча.
В основном лучевая терапия проводится в размере одной фракции в 1,8-2,0 Гр в день, пять дней в неделю. Для быстро растущих опухолей большее теоретическое преимущество дает ускоренная терапия (больше, чем одна фракция в день). Кроме того, лучевая нагрузка в низких дозах позволяет дать более высокую суммарную дозу с меньшим воздействием на неизмененные ткани (гиперфракционированая лучевая терапия) с лучшим воздействием на опухоль. Это может быть эффективно при некоторых опухолях у детей. У взрослых не было выявлено преимуществ ни ускоренного, ни гиперфракционированого облучения.
в) Новейшие разработки:
1. Конформная лучевая терапия. Конформная лучевая терапия подразумевает формирование пучка по размеру и контуру опухоли. Это достигается с помощью (микро) многолепесткового коллиматора или блоков литого свинца.
2. Модуляции интенсивности лучевой терапии. Обычно интенсивность дозы облучения по ходу пучка одинакова. При использовании нескольких пучков с неоднородными (с модуляцией интенсивности) профилями можно сформировать единую дозу в очень сложной (даже вогнутой) области. Это имеет свои преимущества при работе рядом с чувствительными или жизненно важными структурами или когда желательно неоднородное распределение дозы.
3. Стереотаксическая радиохирургия/лучевая терапия. Стереотаксис в лучевой терапии означает лечение поражений, локализованных по отношению к внешней системе координат. При адекватной фиксации пациента стереотаксическое излучение может быть доставлено с точностью менее чем 1 мм. Используя эту методику, можно вывести жизненно важные структуры из пучка. Стереотаксическая радиохирургия (СРХ) подразумевает однократное применение абляционной дозы радиации.
4. Чувствительность к облучению. Было опробовано множество веществ, которые теоретически должны повышать чувствительность опухолевой ткани к излучению. К ним относятся сенсибилизаторы, действующие на субклеточном уровне, такие как IUdR и мизонидазол. Ни один из них не оказался эффективным.

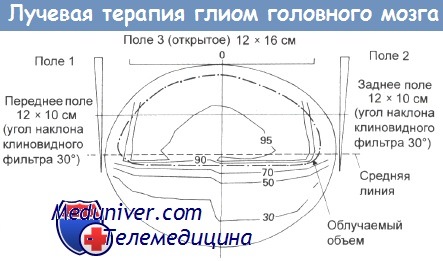
Облучение глиомы коры мозга внешним пучком.
Трехпольное облучение всего полушария мозга. Облучаемый объем показан пунктирной линией.
г) Стандартные подходы к лучевой терапии:
1. Глиомы высокой степени злокачественности. Лучевая терапия увеличивает выживаемость пациентов с недавно диагностированной глиомой высокой степени злокачественности (ГВСЗ). Для оптимизации лечения таких больных учитываются такие прогностические факторы, как возраст, общее состояние, точное гистологическое заключение и, в меньшей степени, размер опухоли и резектабельность. Пациенты с большими шансами на эффективность терапии должны проходить максимальное облучение, в то время как при плохом прогнозе можно дать короткий курс лучевой терапии или вообще его не проводить.
Лечение должно быть проведено сразу же после операции. Высокие дозы излучения локализуют в области резекции с добавлением около 2 см от ее края. Облучение большого объема мозга без необходимости больше не считается необходимой. Резекция опухоли может улучшить устойчивость к радиации и снизить потребность в стероидах, которые часто приходится назначать при лучевой терапии.
Максимальное стандартное лечение составляет 56-66 Гр в течение 5-7 недель. Нет подтверждения, что увеличение интенсивности лечения с помощью интерстициальной лучевой терапии, стереотаксической радиохирургии или с помощью альтернативных схем фракционирования улучшает результаты.
Пациентам с неблагоприятным прогнозом может быть предложен короткий курс облучения (например, 30 Гр за шесть фракций).
Было установлено, что прием темозоломида во время и после лучевой терапии улучшает выживаемость у пациентов с глиобластомой. В этом исследовании двухлетняя выживаемость увеличилась с 10 до 26% с улучшением «времени до прогрессирования» без ущерба для качества жизни. У пациентов с хорошим статусом, перенесших удаление опухоли, лучевая терапия наиболее эффективна. Этот сопутствующий/адъювантный режим сейчас принят в качестве стандарта лечения пациентов с глиобластомой во многих странах.
2. Астроцитомы низкой степени злокачественности. По общему опыту, лечение может вызвать регресс глиом низкой степени злокачественности и улучшить клиническое состояние. Тем не менее, ее роль менее ясна, чем при ГВСЗ. По данным крупномасштабного исследования EORTC и RTOG было установлено, что лучевая терапия не улучшает выживание, но увеличивает время до прогрессирования опухоли. Средняя доза (45 Гр) является столь же эффективной, как и более высокие дозы (60 Гр). Кроме того, выяснилось, что факторы риска являются прогностическими для пациентов, способных выиграть от такого лечения.
Пациенты с хорошим прогностическим показателем (удовлетворительное состояние, возраст < 50, размер опухоли < 6 см, опухоли не связанные со средней линией) после первоначального диагноза могут находиться под наблюдением. Когда планируется лучевая терапия, зона облучения должна включать в себя всю область опухоли, плюс 1-2 см по краю. Общая доза облучения должна быть не более 54 Гр (обычно 50 Гр), не более 1,8 Гр за фракцию.
3. Опухоли, обладающие большим потенциалом метастатазирования. Некоторые опухоли распространяются с током спинномозговой жидкости (например, ПНЭО, некоторые герминоклеточные опухоли). Для них может быть необходимо облучение и спинного мозга. Дозы облучения должны быть равномерно распределены по всей поверхности оболочек и их содержимого с увеличением дозы в областях первичной опухоли и скопления метастазов.
Планирование должно осуществляться с помощью КТ и настроено на максимальную протекцию, чтобы снизить риск повреждения жизненно важных структур и отдаленных осложнений. Обычно проводится параллельное облучение полей мозга и нижней части позвоночника с совмещением одиночного заднего поля позвоночника. Стандартное лечение медуллобластомы без химиотерапии включает облучение всего спинного и головного мозга в дозе 30-35 Гр и опухоли в дозе 55 Гр. Доза может быть снижена при сочетании с химиотерапией. Совершенствование лечения является задачей современных исследований.
4. Радиотерапия доброкачественных опухолей. Некоторые доброкачественные опухоли чувствительны к лучевой терапии (менингиома, аденома гипофиза, краниофарингиома). Долгосрочные перспективы выживания хороши, поэтому, при наведении и дозировке необходима особая точность, для чего в соответствующих случаях может использоваться стереотаксическое наведение IMRT и некомпланарное планирование. Минимальная эффективная фракционная доза составляет не менее 2 Гр. В некоторых случаях может быть использована СРХ.
5. Метастазы. Лучевая терапия является одним из основных методов в лечении метастазов головного мозга, но, возможно, ею отчасти злоупотребляют. Отбор пациентов должн быть основан на принятой схеме классификации. У пациентов с множественными метастазами и тяжелым соматическим статусом, вероятно, преимуществ от лечения не достигается. Молодые пациенты с лучшим состоянием должны получать короткие курсы облучения (20 Гр за пять фракций в течение одной недели).
Пациенты с солитарными (или несколькими) метастазами в головном мозгу, особенно если контролируется системное заболевание, оцениваются в отношении возможности радикального лечение. Хирургия и стереотаксическая радиохирургия (СРХ) в этом случае имеют схожую эффективность. Облучение всего головного мозга снижает риск рецидива и является полезным дополнением.
д) Отдаленные последствия лучевой терапии. Здоровая ткань мозга, прилегающая к опухоли, неизбежно подвергается риску повреждения. Наиболее важные изменения происходят достаточно поздно после облучения (от 6 месяцев до 10 лет) и включают изменения белого вещества, повреждение сосудов, нейронов, глиоз и кальцификации. Клинические проявления могут варьировать от незначительного ухудшения когнитивных функций до грубого неврологического дефицита. Риск после тщательно взвешенного и дозированного облучения, очевидно, преувеличивается.
У пациентов с глиомами низкой степени злокачественности отдаленные последствия могут быть умеренными по сравнению со случаями дефицита перед облучением. У пациентов с предшетвующими нарушениями когнитивных функций после лучевой терапии может наблюдаться их улучшение.
е) Клинические и научные разработки лучевой терапии опухоли головного мозга:
1. Протоны. В протонном пучке наибольшее количество энергии выделяется на последних нескольких миллиметрах пути, известном как «максимум Брэгга». Это свойство можно использовать для доставки в опухоли больших доз облучения, в том числе находящихся в непосредственной близости от жизненно важных структур. Наиболее распространенной областью применения в ЦНС являются хордомы ската черепа и другие опухоли основания черепа. Однако данная технология очень дорога и доступна в очень немногих центрах.
2. Брахитерапия. Брахитерапия основана на использовании временных имплантов с высокой активностью (125I) и применялась при глиомах высокой степени злокачественности при рецидиве или первичном лечении. Однако результаты не подтвердили эффективность брахитерапии. Импланты также применялись для лечения глиом низкой степени злокачественности, а иридиевая проволока в качестве паллиативного средства при глиобластоме.
3. Терапия методом захвата нейтронов бором. Терапия методом захвата нейтронов бором заключается в захвате и взаимодействии нейтронов с очень низкой энергией (тепловой) или с низкой энергией (эпитермальной) стабильным изотопом бора-10 (10В). Захват вызывает распад 10В и высвобождение а-частиц и частиц лития.
N + 10В -» 4Не + 7Li
Успех методики заключается в селективном накоплении 10В в опухоли при использовании меченых соединений бора, таких как 10B-BSA. Пучок низкоэнергетических нейтронов с высокой линейной энергетической передачей (LET) обладает малым рассеиванием около опухоли. Это метод изучается в нескольких центрах мира.
ж) Будущее лучевой терапии ЦНС. Лучевая терапия — один из основных методов лечения у больных с различными опухолями ЦНС, особенно злокачественными. Это положение будет сохраняться и в обозримом будущем. Тем не менее, мы приближаемся к пределу, за которым технические улучшения доставки излучения дают небольшие дополнительные преимущества. Перспектива совершенствования методов возникнет на основе нашего лучшего понимания механизмов контролирования клеточного цикла и реагирования на радиационное облучение.
– Также рекомендуем “Схема химиотерапии опухоли головного мозга – Европейские протоколы”
Оглавление темы “Нейрохирургия опухоли головного мозга.”:
- Схема лучевой терапии опухоли головного мозга – Европейские рекомендации
- Схема химиотерапии опухоли головного мозга – Европейские протоколы
- Схема адъювантного лечения опухоли мозга у ребенка – Европейские рекомендации
- Схема адъювантной терапии злокачественной глиомы головного мозга у ребенка – Европейские рекомендации
- Схема адъювантной терапии медуллобластомы у ребенка – Европейские рекомендации
- Схема адъювантной терапии эпендимомы у ребенка – Европейские рекомендации
- Новые методы лечения опухоли головного мозга и их эффективность
- Алгоритм диагностики аневризмы сосуда головного мозга – Европейские рекомендации
Источник
