Ангионевротический отек анализы крови

Медицинский эксперт статьи
х
Весь контент iLive проверяется медицинскими экспертами, чтобы обеспечить максимально возможную точность и соответствие фактам.
У нас есть строгие правила по выбору источников информации и мы ссылаемся только на авторитетные сайты, академические исследовательские институты и, по возможности, доказанные медицинские исследования. Обратите внимание, что цифры в скобках ([1], [2] и т. д.) являются интерактивными ссылками на такие исследования.
Если вы считаете, что какой-либо из наших материалов является неточным, устаревшим или иным образом сомнительным, выберите его и нажмите Ctrl + Enter.
Ангионевротический отек – это отек глубоких слоев дермы и подкожных тканей. Он может быть вызван лекарственными препаратами, ядом (особенно животного происхождения), пищевыми или экстрактированными аллергенами. Главный симптом – диффузный, болезненный отек, иногда ограниченный. Диагноз основан на общем осмотре. Лечение направлено на элиминацию или отмену аллергена и назначение Н2-блокаторов.
[1], [2], [3], [4], [5], [6], [7], [8], [9], [10]
Код по МКБ-10
T78.3 Ангионевротический отек
Причины ангионевротического отека
Острый ангионевротический отек практически представляет собой анафилактическую реакцию подкожных тканей. Иногда он сопровождается уртикарной сыпью (локализованные волдыри и эритема на коже); в обоих случаях причины схожие (например, лекарственные препараты, яды, пищевые и экстрагированные аллергены). Ангиневротический отек патогенетически связан с крапивницей, которая проявляется на уровне эпидермально-дермального соединения.
Хронический (> 6 недель) ангионевротический отек в редких случаях является lgE-опосредованным, чаще – трудно объяснимым нарушением. Причина обычно неизвестна (идиопатический отек), но иногда причиной является хроническое употребление не вызывающих опасений лекарственных препаратов или иных синтетических продуктов (пенициллин в молоке, лекарства безрецептурного отпуска, консерванты, другие пищевые добавки). В некоторых случаях ангионевротический отек является врожденным.
[11], [12], [13], [14], [15], [16]
Симптомы ангионевротического отека
При ангионевротическом отеке может отмечаться (либо отсутствовать) легкий зуд. Это состояние характеризуется ограниченным диффузным и болезненным отеком мягких тканей, который может быть ассиметричным; особенно подвержены отеку области век, губ, лица, языка, а также тыльная сторона рук и ног, гениталии. Отек верхних дыхательных путей может вызвать респираторный дистресс, и стридор иногда ошибочно принимают за астму. Может иметь место полная обструкция дыхательных путей.
Диагностика ангионевротического отека
Причина зачастую является очевидной, и диагностические тесты проводятся редко, так как реакции самостоятельно купируются и не рецидивируют. Никакие тесты не являются особенно необходимыми для диагностики. Эритропоэтическая протопорфирия может маскироваться под аллергические формы ангионевротического отека и диагностируется путем измерения количества порфиринов в крови и фекалиях.
[17], [18], [19], [20], [21], [22], [23], [24]
Какие анализы необходимы?
Лечение ангионевротического отека
В случае острого ангионевротического отека лечение заключается в устранении или избегании аллергена и назначении симптоматических препаратов (например, Н2 -блокаторов). В наиболее тяжелых случаях назначается преднизолон 30-40 мг однократно в день. Местная терапия глюкокортикоидами бесполезна. Если причина не очевидна, необходимо прекратить прием всех второстепенных препаратов. При отеке глотки или гортани назначают эфедрин 0,3 мл в растворе 1:1000 подкожно. Лечение может быть дополнено внутривенным введением антигистаминных препаратов (дифенгидамин 50-100 мг). Длительное лечение может включать назначение Н1 – и Н2-блокаторов и иногда глюкокортикоидов.
Н1-блокаторы для перорального применения
Препарат | Дозировка для взрослых | Дозировка для детей | Доступные лекарственные формы |
Азатадин малеат | 1-2 мг 2 раза в день | > 12 лет: во взрослой дозировке | Таблетки 1 мг |
Бромфенирамин малеат | 4 мг каждые 4-6 ч или 8 мг каждые 8-12 ч | 6-12 лет: 2-4 мг каждые 6-8 ч (максимальная доза 12-16 мг вдень). > 12 лет: во взрослой дозировке | Таблетки 4, 8, 12 мг. Эликсир 2 мг/5 мл. Таблетки 8,12 мг (пролонгированного действия) |
Хлорфенирамин малеат | 2-4 мг каждые 4-6 ч | 6-11 лет: 2 мг каждые 4-6 ч (максимальная доза 12-16мг/день). > 12 лет: во взрослой дозировке | Жевательные таблетки 2 мг. Таблетки 4, 8, 12 мг. Сироп 2 мг/5 мл. Таблетки или капсулы 8, 12мг |
Клемастин фумарат | От 1,34 мг 2 раза в день до 2,68 мг 3 раза в день | 6-12 лет: 0,5 мг каждые 12 ч (максимальная доза 3 м г/день)3 | Таблетки 1,34; 2,68 мг. Сироп 0,67 мг/5 мл |
Ципрогептадин HCI | 4 мг 3 или 4 раза в день [максимальная доза 0,5 мг/(кгхдень)] | 2-6 лет: 2 мг 2 или 3 раза в день (максимально 12мг/день). 7-14 лет: 4 мг 2 или 3 раза в день (максимально 16мг/день) | Таблетки 4 мг. Сироп 2 мг/5 мл |
Дексхлорфенирамина малеат | 2 мг каждые 4-6 ч | 2-5 лет: 0,5 мг каждые 4-6 ч (максимальная доза 3 мг/день). 6-11 лет: 1 мг через 4-6 ч (максимальная доза 6 мг/ день) | Таблетки 2 мг. Сироп 2 мг/5 мл. Таблетки 4,6 мг. (пролонгированного действия) |
Дифенгидрамин | 25-50 мг каждые 4-6 ч | 1,25 м г/кг каждые 6 ч (максимальная доза 300 мг/день) | Капсулы или таблетки 25, 50 мг. Сироп 12,5мг/мл. Эликсир 12,5/5 мл |
Дифенилпиралин | 5 мг каждые 12 ч | Данных нет | Капсулы 5 мг(пролонгированного действия) |
Гидроксизин HCI | 25-50 мг 3 или 4 раза в день | 0,7 мг/кг 3 раза в день | Капсулы 25, 50,100 мг. Таблетки 10,25,50 и 100 мг. Сироп 10 мг/5 мл. Оральная суспензия 25 мг/5 мл |
Метдилазин HCI | 8 мг каждые | > 3 лет: 4 мг каждые | Таблетки 8 мг. Жевательные таблетки 4 мг. Сироп 4 мг/5 мл |
Прометазин HCI | 12,5-25 мг 2 раза в день | 2 лет: 6,25-12,5 мг 2 или 3 раза в день | Таблетки 12,5; 25;50 мг. Сироп 6,25 и 25 мг/5 мл |
Тримепразина тартрат | 2,5 мг 4 раза | 6 мес -3 года: 1,25 мг на ночь или 3 раза в день. > 3 лет: 2,5 мг на ночь или 3 раза в день | Таблетки 2,5 мг. Сироп 2,5 мг/5 мл . Капсулы 5 мг (пролонгированного действия) |
Трипеленнамина цитрат | 25-50 мг каждые 4-6 ч | 1,9 мг/кг 4 раза в день (максимально 450 мг/ в день) | Эликсир 37,5 мг/5 мл (1 мл цитрата=5 мг соли HCI) |
Трипеленнамин HCI | 25-50 мг каждые 4-6 ч | 1,25 мг/кг 4 раза в день (максимально 300 мг/ в день) | Таблетки 25; 50 мг. Таблетки 100мг (пролонгированного действия) |
Трипролидин HCI | 2,5 мг каждые 4-6 ч (максимально 10 мг/день) | 4 мес – 2 года: 0,313 мг каждые 4-6 ч (макси мально 1,25 мг/день). 2-4 года: 0,625 мг каждые 4-6 ч (максимально 2,5 мг/день). 4-6 лет: 0,938 мг каждые 4-6 ч (максимально 3,744 мг/день). 6-12 лет: 1,25 мг каждые 4-6 ч (максимально 5 мг/день) | Таблетки 2,5 мг. Сироп 1,25 мг/5 мл |
Без седативного эффекта
Препарат | Дозировка для взрослых | Дозировка для детей | Доступные лекарственные формы |
Акривастин | 8 мг 2 или 3 раза | 12 лет: во взрослой дозировке | Капсулы 8 мг |
Цетиризин | 5-10 мг 1 раз | > 12 лет: во взрослой дозировке | Таблетки 5,10 мг |
Деслоратадин | 5 мг 1 раз в день | > 12 лет: во взрослой дозировке | Таблетки 5 мг |
Эбастин | 10-20 мг 1 раз вдень | 6-12 лет: 5 мг. 12-17 лет: 5-20 мг 1 раз в день | Таблетки 10 мг |
Фексофенадин | 60 мг 2 раза в день или 180 мг 1 раз в день | 6-11 лет: 30 мг 2 раза вдень. 12 лет: во взрослой дозировке | Таблетки 60,180 мг |
Левоцетиризин | 5 мг 1 раз в день | Данных нет | Таблетки 5 мг |
Лоратадин | 10 мг 1 раз | 2-5 лет: 5 мг 1 раз в день. 6 лет: во взрослой дозировке | Таблетки 10 мг. Сироп 1 мг/1 мл |
Мизоластин | 10 мг 1 раз | Данных нет | Таблетки 10 мг |
У всех антигистаминных препаратов с седативным эффектом отмечаются антихолинергические свойства. Они, как правило, не используются у пожилых людей и у пациентов с глаукомой, доброкачественной гиперплазией простаты, делирием, деменцией и ортостатическои гипотензиеи. При приеме этих препаратов отмечаются сухость во рту, снижение четкости зрения, задержку мочи, запор, ортостатическую гипотензию.
Источник
Наследственный ангионевротический отек – генетическое заболевание, при котором наблюдается дефицит ингибитора С1-компонента комплемента. Симптомами являются рецидивирующие отеки кожи, слизистых оболочек и органов брюшной полости, которые могут сопровождаться удушьем (при отеке гортани), рвотой и болями в животе (при поражении брюшной полости). Диагностика производится на основании осмотра, изучения наследственного анамнеза, определения С1-ингибитора, компонентов С4 и С2 в плазме крови, молекулярно-генетических исследований. Лечение осуществляется путем компенсирования абсолютного или функционального дефицита С1-ингибитора, применения блокаторов брадикинина и калликреина, использования свежезамороженной донорской плазмы.
Общие сведения
Наследственный ангионевротический отек (НАО) – вариант первичного иммунодефицита, обусловленный нарушением ингибирования системы комплемента, точнее, его основной фракции С1. Впервые это состояние было описано в 1888 году У. Осиером, который выявил рецидивирующие отеки у молодой женщины, а также установил, что подобное заболевание имелось как минимум у пяти поколений ее семьи. Примечательно, что собственно ангионевротический отек был открыт И. Квинке всего за 6 лет до обнаружения наследственной формы этой патологии – в 1882-м году. Наследственный ангионевротический отек имеет аутосомно-доминантный характер передачи и с одинаковой частотой поражает как мужчин, так и женщин. По некоторым данным, у женщин заболевание протекает тяжелее и возникает раньше, однако достоверных исследований по этому поводу не производилось. Встречаемость наследственного ангионевротического отека, по всей видимости, значительно варьирует у разных этнических групп, что дает весьма неоднородные цифры этого показателя – от 1:10 000 до 1:200 000.
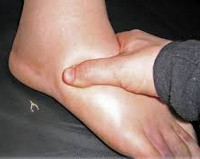
Наследственный ангионевротический отек
Причины наследственного ангионевротического отека
Непосредственной причиной развития наследственного ангионевротического отека является первичный иммунодефицит, заключающийся в дефиците или функциональной неполноценности ингибитора эстеразы одного из компонентов комплемента – С1. В результате этого также нарушается ингибирование активации других компонентов этой системы – С4 и С2, что приводит к еще большему расстройству работы данного иммунного механизма. Врачам-генетикам удалось установить ген, отвечающий за 98% форм наследственного ангионевротического отека – им является C1NH, расположенный на 11-й хромосоме и кодирующий вышеуказанный ингибитор эстеразы С1. Различные мутации способны приводить к неодинаковым по своему течению формам заболевания, которые обладают достаточно сходными клиническими проявлениями, но различаются при проведении ряда диагностических тестов.
При одних типах мутации гена C1NH происходит полное прекращение синтеза белка-ингибитора С1, в результате чего он отсутствует в плазме крови, а остановка системы комплемента производится малоэффективными побочными путями. В других случаях наследственный ангионевротический отек возникает на фоне нормального содержания ингибитора в крови, при этом генетический дефект C1NH приводит к нарушению структуры активного центра данного фермента. В результате ингибитор С1 становится функционально неполноценным, что и служит причиной развития патологии. Существуют также редкие формы наследственного ангионевротического отека, при которых не наблюдается как изменений количества или активности ингибитора эстеразы С1, так и мутаций в гене C1NH – этиология и патогенез таких заболеваний на сегодняшний день неизвестны.
Остановка ингибирования активности компонентов комплемента (С1, С2, С4) приводит к запуску иммунной реакции, сходной по своему течению с аллергической, особенно крапивницей. Компоненты комплемента способны расширять кровеносные сосуды глубоких слоев дермы, повышать проницаемость их стенок, что провоцирует диффундирование компонентов плазмы крови в межклеточное пространство тканей кожи и слизистых оболочек и приводит к их отеку. Кроме того, немаловажную роль в патогенезе наследственного ангионевротического отека играют вазоактивные полипептиды – брадикинин и калликреин, которые еще больше увеличивают степень отека, а также способны вызывать спазм гладкомышечной мускулатуры органов желудочно-кишечного тракта. Эти процессы обуславливают все разнообразие симптомов наследственного ангионевротического отека: отечность кожи (в области конечностей, лица, шеи) и слизистых оболочек (ротовой полости, гортани, глотки), боли в животе и диспепсические расстройства, провоцируемые сочетанием отеков и спазмов.
Классификация наследственного ангионевротического отека
Всего на сегодняшний день выявлено три основных типа наследственного ангионевротического отека. Их различия в плане клинического течения патологии очень незначительны, для определения формы заболевания используют специальные диагностические методики. Врачу-иммунологу крайне важно выяснить тип наследственного ангионевротического отека, так как от этого во многом зависит тактика лечения данной патологии:
- Наследственный ангионевротический отек 1-го типа (НАО-1) – является наиболее распространенной формой заболевания, регистрируется у 80-85% больных с такой патологией. Причиной НАО этого типа является отсутствие гена C1NH или нонсенс-мутация в нем, в результате чего ингибитор С1 не образуется в организме.
- Наследственный ангионевротический отек 2-го типа (НАО-2) – более редкая форма патологии, выявляется лишь у 15% больных. Обусловлен также генетическим дефектом в C1NH, однако при этом экспрессия белка-ингибитора С1 не останавливается, а сам фермент имеет измененную структуру своего активного центра. Это приводит к его неполноценности, и он становится неспособен правильно выполнять свои функции.
- Наследственный ангионевротический отек 3-го типа – относительно недавно обнаруженная форма заболевания с практически неизученными этиологией и патогенезом. Достоверно удалось выяснить, что при этом типе отека отсутствуют мутации гена C1NH, сохраняется нормальное количество ингибитора эстеразы компонента комплемента С1 и его функциональная активность. Больше никаких данных по поводу данной формы (или их совокупности) наследственного ангионевротического отека не имеется.
Симптомы наследственного ангионевротического отека
Как правило, при рождении и в детском возрасте (за исключением редких случаев) наследственный ангионевротический отек ничем себя не проявляет. Довольно часто первые признаки заболевания возникают в подростковом периоде, так как их провоцируют стрессы и гормональные перестройки, происходящие в организме в это время. Однако нередко наследственный ангионевротический отек появляется позже – в возрасте 20-30 лет или даже у пожилых лиц. Чаще всего развитию первого приступа предшествует какое-либо провоцирующее явление: мощный эмоциональный стресс, серьезное заболевание, хирургическое вмешательство, прием некоторых лекарственных средств. В дальнейшем «порог чувствительности» по отношению к провоцирующим факторам снижается, приступы возникают все чаще – наследственный ангионевротический отек приобретает рецидивирующий характер.
Основным проявлением заболевания у большинства больных является отек кожи и подкожной клетчатки на кистях, стопах, иногда лице и шее. В более тяжелых случаях отечные явления возникают на слизистых оболочках полости рта, гортани и глотки – при этом может развиваться удушье (асфиксия), являющееся наиболее частой причиной смерти от наследственного ангионевротического отека. В других случаях на первый план выступают симптомы со стороны желудочно-кишечного тракта: тошнота, рвота, боли и рези в животе, иногда подобная клиническая картина приобретает черты «острого живота». В отдельных случаях наследственный ангионевротический отек характеризуется сочетанием отека кожи, слизистых оболочек и поражения желудочно-кишечного тракта.
Диагностика наследственного ангионевротического отека
Для выявления наследственного ангионевротического отека используют данные физикального осмотра больного, изучения его наследственного анамнеза, определения в крови количества ингибитора С1, а также компонентов комплемента С1, С2, С4, и молекулярно-генетических исследований. Осмотр в фазу обострения заболевания выявляет отек кожи или слизистых оболочек, пациенты могут жаловаться на боли в животе, рвоту, диарею. В крови при наличии наследственного ангионевротического отека 1-го типа ингибитор эстеразы С1 полностью отсутствует, значительно снижены концентрации индикаторных компонентов комплемента. При 2-м типе заболевания в плазме крове может определяться незначительное количество ингибитора С1, в редких случаях его уровень соответствует норме, но соединение имеет пониженную функциональную активность. При всех трех вариантах наследственного ангионевротического отека уровень С1, С2 и С4 не превышает 30-40% от нормы, поэтому этот показатель является ключевым в диагностике данного состояния.
Изучение наследственного анамнеза пациента зачастую обнаруживает наличие подобного заболевания как минимум у нескольких поколений его предков и у других родственников. Однако отсутствие признаков семейного характера патологии не является однозначным критерием, позволяющим исключить наследственный ангионевротический отек – примерно у четверти больных это состояние обусловлено спонтанными мутациями и выявляется впервые в семье. Молекулярно-генетическая диагностика осуществляется путем автоматического секвенирования гена C1NH с целью выявления мутаций. Дифференциальную диагностику следует производить с ангионевротическим отеком аллергического генеза и приобретенными формами дефицита ингибитора С1.
Лечение наследственного ангионевротического отека
Терапию наследственного ангионевротического отека разделяют на два типа – лечение для купирования острого приступа заболевания и профилактический прием препаратов для предупреждения их развития. В случае острого отека Квинке, обусловленного НАО, традиционные противоанафилактические меры (адреналин, стероиды) неэффективны, необходимо использовать нативный или рекомбинантный ингибитор С1, антагонисты брадикинина и калликреина, при их отсутствии показано переливание свежезамороженной плазмы. Начинать такое лечение нужно как можно раньше, в идеале – при самых первых приступах наследственного ангионевротического отека.
Долгосрочная профилактика заболевания производится в тех случаях, когда приступы возникают слишком часто (чаще раза в месяц), если в анамнезе имелись случаи отека гортани или удушья, либо госпитализация в реанимационное отделение. Профилактика включает в себя использование андрогенов, экзогенных (рекомбинантных или нативных) форм ингибитора эстеразы С1, антифибринолитических препаратов. При доброкачественном течении наследственного ангионевротического отека – редких приступах и их относительно быстром исчезновении – такое лечение может не назначаться. Однако накануне хирургических или стоматологических вмешательств, физических и умственных нагрузок рекомендуется краткосрочно принимать вышеуказанные средства для уменьшения риска развития приступа.
Прогноз и профилактика наследственного ангионевротического отека
В большинстве случаев прогноз наследственного ангионевротического отека относительно благоприятный в плане выживаемости – при разумном лечении и профилактике приступы возникают крайне редко и не угрожают жизни больного. При этом всегда сохраняется риск отека гортани, что может привести к асфиксии и летальному исходу. Таким больным следует не только избегать значительных физических и эмоциональных нагрузок, но и желательно иметь при себе карточку или медальон с указанием диагноза. Огромное количество смертей от наследственного ангионевротического отека было обусловлено неверными действиями медиков, не знающих диагноза и поэтому использующих традиционные при аллергическом отеке Квинке препараты, которые неэффективны при НАО.
Источник
